ビフィズス菌が母乳のオリゴ糖を分解する酵素のかたちと反応メカニズムを解明
- 発表者
-
伊藤 佑 (東京大学大学院農学生命科学研究科応用生命工学専攻 博士課程3年)
片山 高嶺 (石川県立大学生物資源工学研究所 准教授)
Mitchell Hattie (University of Western Australia 大学院生)
櫻間 晴子 (石川県立大学生物資源工学研究所 博士研究員;当時)
和田 潤 (京都大学大学院生命科学研究科 博士課程;当時)
鈴木 龍一郎 (東京大学大学院農学生命科学研究科応用生命工学専攻 博士研究員;当時)
芦田 久 (近畿大学生物理工学部 教授)
若木 高善 (東京大学大学院農学生命科学研究科応用生命工学専攻 教授;当時)
山本 憲二 (石川県立大学生物資源工学研究所 教授)
Keith A. Stubbs (University of Western Australia 准教授)
伏信 進矢 (東京大学大学院農学生命科学研究科応用生命工学専攻 教授)
発表のポイント
◆ ヒトの母乳に含まれる複雑なオリゴ糖から「ラクトNビオース」と呼ばれる二糖を切り取るはたらきを持つ、ビフィズス菌の表面にある酵素の立体的なかたちを明らかにしました。
◆ この酵素がどのようにラクトNビオースを捕まえて、切断するか、というメカニズムの詳細を解明しました。
◆ この酵素は乳児の腸内に生息するビフィズス菌から見つかっており、ラクトNビオースはビフィズス菌を増やす増殖因子としての機能が明らかになっています。この酵素を改変して利用することにより、ビフィズス菌の増殖因子を合成することが可能になると期待できます。
発表概要
ビフィズス菌はヒトの腸管内に生息し、宿主にとって有益な「善玉菌」として知られている。また、母乳栄養乳児の腸内にはビフィズス菌が速やかに定着することが古くから知られている。
近年の研究により、ヒトの母乳中に含まれる複雑な構造のオリゴ糖(ヒトミルクオリゴ糖:注1)にビフィズス菌を増殖させる因子「ラクトNビオース(注2)」が豊富に存在していること、さらに、ビフィズス菌の表面にある「ラクトNビオシダーゼ(注3)」という酵素が、ヒトミルクオリゴ糖からラクトNビオースを切り出すはたらきをすることが分かってきた。しかし、ラクトNビオシダーゼがラクトNビオースのみを切り出す詳細なメカニズムは分かっていなかった。
今回、東京大学大学院農学生命科学研究科の伏信進矢教授らの研究グループは、ラクトNビオシダーゼの三次元構造を、X線結晶構造解析(注4)により初めて明らかにした。ラクトNビオシダーゼの中央には、ラクトNビオースの2つの糖がぴったりとはまるポケットがあった。本研究では、高エネルギー加速器研究機構(KEK)物質構造科学研究所のフォトンファクトリー(注5)を利用して測定を行い、ラクトNビオースと、強力な阻害剤(注6)である「ラクトNビオース-チアゾリン」が、そのポケットに結合した構造を、高分解能で決定することに成功した。ラクトNビオシダーゼに結合したラクトNビオースと阻害剤の形状から、この酵素が触媒反応を行う際の詳細なメカニズムが明らかになった。ラクトNビオシダーゼは乳児の腸内に生息するビフィズス菌から見つかっており、今後、この酵素を改変して利用することにより、ビフィズス菌の増殖因子を合成することが可能になると期待できる。
発表内容
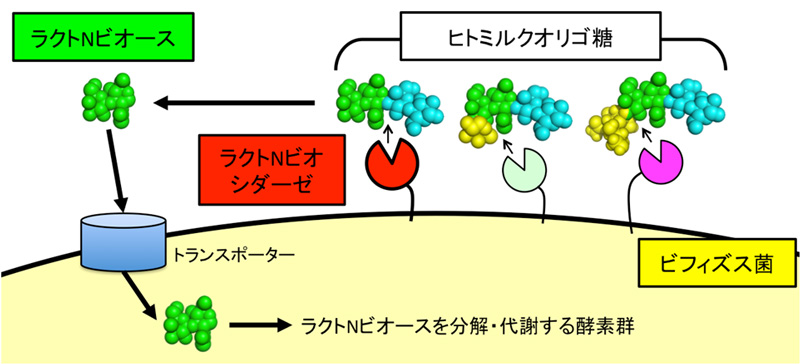
図1: ビフィズス菌のヒトミルクオリゴ糖代謝経路(概念図) (拡大画像↗)
ビフィズス菌(B. bifidum JCM1254株)の菌体外にはヒトミルクオリゴ糖を切断する酵素が複数発見されているが、そのうち、ラクトNビオシダーゼ(赤色)は、ラクトNビオース(緑色)を切り出す酵素である。さらに、ビフィズス菌は、遊離したラクトNビオースを菌体内に取り込むトランスポーターと、菌体内でラクトNビオースを分解代謝する一連の酵素を持つことが分かっている。
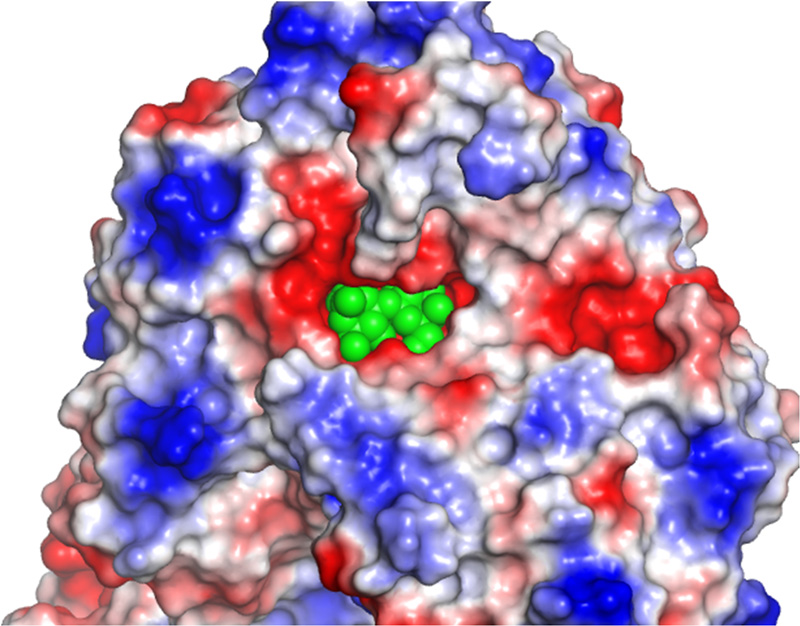
図2: ラクトNビオシダーゼに結合したラクトNビオース (拡大画像↗)
ラクトNビオシダーゼの分子表面の正電荷を青で、負電荷を赤で表す。ラクトNビオース(緑色)がぴったりとはまるポケットが分子の中央に存在する。
ビフィズス菌はヒトの腸管内に生息し、宿主にとって有益な「善玉菌」として知られています。また、母乳栄養乳児の腸内にはビフィズス菌が速やかに定着することが古くから知られています。ヒトの母乳には10?20 g/L程度の複雑な構造を持つオリゴ糖(ヒトミルクオリゴ糖)が含まれており、これにビフィズス菌を増殖させる因子が含まれていることは分かっていましたが、近年までその実体は明らかになっていませんでした。2005年に、農業・食品産業技術総合研究機構食品総合研究所の北岡本光博士らにより、ビフィズス菌からヒトミルクオリゴ糖に含まれる二糖であるラクトNビオースを分解する一連の酵素の遺伝子が発見されました。その後の研究で、ラクトNビオースはビフィズス菌を選択的に増殖させる因子であることが明らかになっています。また、帯広畜産大学の浦島匡教授らは、ヒトミルクオリゴ糖にはラクトNビオースが含まれるタイプのオリゴ糖が多く含まれており、他のほ乳類の乳では、類人猿においてさえも、ラクトNビオースが含まれるタイプのオリゴ糖はまったく含まれないか、あったとしても少量であることを明らかにしています。すなわち、ヒトの乳幼児の腸管に生息するビフィズス菌は母乳に豊富に含まれるラクトNビオースを栄養源として利用していると推測されます。しかし、ヒトミルクオリゴ糖には、ラクトNビオースの二糖そのものは含まれておらず、かならず他の糖と結合したかたちでしか存在していません。そのような背景のもと、2008年に、京都大学(当時)の山本憲二教授らのグループは、ビフィズス菌から、ヒトミルクオリゴ糖のラクトNビオース部分だけを切り出す酵素「ラクトNビオシダーゼ」を発見しました。すなわち、この酵素は、ビフィズス菌が、ヒトミルクオリゴ糖から、増殖因子であるラクトNビオースを切り出す、重要な酵素であると言えます。
本研究では、東京大学大学院農学生命科学研究科の伏信進矢教授、石川県立大学生物資源工学研究所の片山高嶺准教授と山本憲二教授、近畿大学生物理工学部の芦田久教授らのグループが、ラクトNビオシダーゼの三次元構造を、フォトンファクトリーのBL‐17Aを利用し、X線結晶構造解析の技術を用いて高分解能で初めて明らかにしました。また、2011年に豪州・西オーストラリア大学のKeith A. Stubbs准教授らによって開発された強力な阻害剤「ラクトNビオース-チアゾリン」を用いています。
ラクトNビオシダーゼの中央には、ラクトNビオースの2つの糖がぴったりとはまるかたちとサイズを持つポケットがありました。ここには数多くの相互作用が存在し、この酵素がラクトNビオースを厳密に認識している様子が明らかになりました。また、ラクトNビオシダーゼに結合したラクトNビオースと阻害剤の立体配座が観測できたことから、この酵素が触媒反応を行う際に、基質であるヒトミルクオリゴ糖がどのように構造変化をして、切断(分解)されるかという、詳細なメカニズムを推定することができました。
本研究から、ラクトNビオシダーゼのどの部分がヒトミルクオリゴ糖をどのように認識しているのか、触媒反応に重要な部位はどこなのか、といった情報が一気に得られました。従って、この酵素を改変して、逆反応であるヒトミルクオリゴ糖の合成に適した酵素にする、といったような工学的手法が可能になったといえます。また、近年、ヒトの腸内に生息する微生物の全体(ミクロビオーム)の研究が進んでいますが、そこに存在する遺伝子からラクトNビオシダーゼの遺伝子を推定するために重要な情報も得られました。将来的には、健康に寄与する食品の開発などへの応用が期待されます。
発表雑誌
- 雑誌名
- 「The Journal of Biological Chemistry」(288巻17号、(2013年)、11795-11806ページ)
- 論文タイトル
- Crystal Structures of a Glycoside Hydrolase Family 20 Lacto-N-biosidase from Bifidobacterium bifidum
- 著者
- Tasuku Ito, Takane Katayama, Mitchell Hattie, Haruko Sakurama, Jun Wada, Ryuichiro Suzuki, Hisashi Ashida, Takayoshi Wakagi, Kenji Yamamoto, Keith A. Stubbs, and Shinya Fushinobu
- DOI番号
- 10.1074/jbc.M112.420109
- アブストラクト
- http://www.jbc.org/content/288/17/11795
問い合わせ先
東京大学大学院農学生命科学研究科 応用生命工学専攻 酵素学研究室
教授 伏信 進矢
Tel: 03-5841-5151
Fax: 03-5841-5151
E-mail: asfushi@mail.ecc.u-tokyo.ac.jp
用語解説
(注1) ヒトミルクオリゴ糖: 牛乳に含まれるオリゴ糖のほとんどが乳糖(ラクトースとも呼ばれる、ガラクトースとグルコースがβ1,4-結合した二糖)であるのに対し,ヒトの母乳では約20%がラクトース以外の種々のオリゴ糖であり,これらは総称してヒトミルクオリゴ糖と呼ばれている。ヒトミルクオリゴ糖は3糖以上の複雑な構造を持つ約130種類のオリゴ糖の混合物からなる。
(注2) ラクトNビオース: ガラクトースとN-アセチルグルコサミンがβ1,3-結合した二糖。
(注3) ラクトNビオシダーゼ: オリゴ糖の末端に存在するラクトNビオースの部分を加水分解により切断する酵素。乳幼児の腸管内に生息するタイプのビフィズス菌(Bifidobacterium bifidumとBifidobacterium longum)のうち、複数の菌株から発見されている。本研究では、B. bifidum JCM1254株から取得されたラクトNビオシダーゼを用いた。
(注4) X線結晶構造解析: 酵素(タンパク質)の立体構造を得るための最も一般的な方法の一つ。目的物質の結晶にX線を照射し、回折データを測定することにより、微細な三次元構造を知ることが出来る。
(注5) 光(Photon)の工場(Factory)の愛称で親しまれているフォトンファクトリー(PF)は、日本初のX線を利用出来る放射光専用光源として1982年に完成した。大学や研究機関が共同で利用実験するための施設(大学共同利用機関)としてKEKで運用され、年間約3千名を超える国内外の研究者が実験に訪れ、物質科学・生命科学の基礎から応用に至る世界最先端の研究成果を創出している。
(注6) 阻害剤: 酵素のはたらきを妨げる分子。本研究で用いた「ラクトNビオース-チアゾリン」は酵素反応の中間体によく似た構造を持ち、ラクトNビオシダーゼの触媒を担う部分に強く結合する。