新規触媒活性を有する麹菌タイプIII型ポリケタイド合成酵素CsyB
- 発表者
-
橋元 誠(岩手医科大学薬学部 助教)
高圓 宰(岩手医科大学薬学部 学部学生(当時))
高橋 宏明(岩手医科大学薬学部 学部学生(当時))
須田 千尋(岩手医科大学薬学部 学部学生)
北本 勝ひこ(東京大学大学院農学生命科学研究科 応用生命工学専攻 教授)
藤井 勲(岩手医科大学薬学部 教授)
発表のポイント
◆麹菌Aspergillus oryzae(注1)由来タイプIII型PKS(ポリケタイド合成酵素polyketide synthase)(注2)であるCsyBが、脂肪酸アシルCoAとマロニルCoA、アセトアセチルCoAから3-アセチル-4-ヒドロキシ-6-アルキル(アルケニル)-α-ピロン(AcAP)を生成することを大腸菌での発現、および組換え酵素を用いた反応解析により明らかにした。
◆CsyBは、2分子β-ケトアシルCoAの縮合反応を触媒する新規タイプIII型PKSであることを明らかにした。
発表概要
糸状菌の全ゲノム解析により、糸状菌にも植物で多く見出されているタイプIII型PKS遺伝子が存在することが確認されています。糸状菌由来のIII型PKSでは6-アルキル-α-ピロンやレゾルシノールなどの芳香族化合物を合成することが報告されていますが、その多くは機能が明らかではありません。東京大学大学院農学生命科学研究科の北本勝ひこ教授、岩手医科大学薬学部の藤井勲教授らの研究グループは大腸菌、および組換え酵素を用いた反応解析により、麹菌由来のIII型PKSであるCsyBが脂肪酸アシルCoA、マロニルCoA、アセトアセチルCoAからAcAPを合成できることを明らかにしました。CsyBは、2分子のβ-ケトアシルCoAの縮合反応を触媒するタイプIII型PKSとして初めての例であり、C4~C18のアルキル鎖(もしくはアルケニル鎖)をもつ脂肪酸アシルCoAが開始基質となり得ること、マロニルCoAとの反応後に生成したβ-ケトアシルCoAと縮合するもう一つのβ-ケトアシルCoAを組み合わせることにより多様なAcAP化合物の生成が可能と考えられ、生成化合物の生理活性にも興味が持たれます。
発表内容
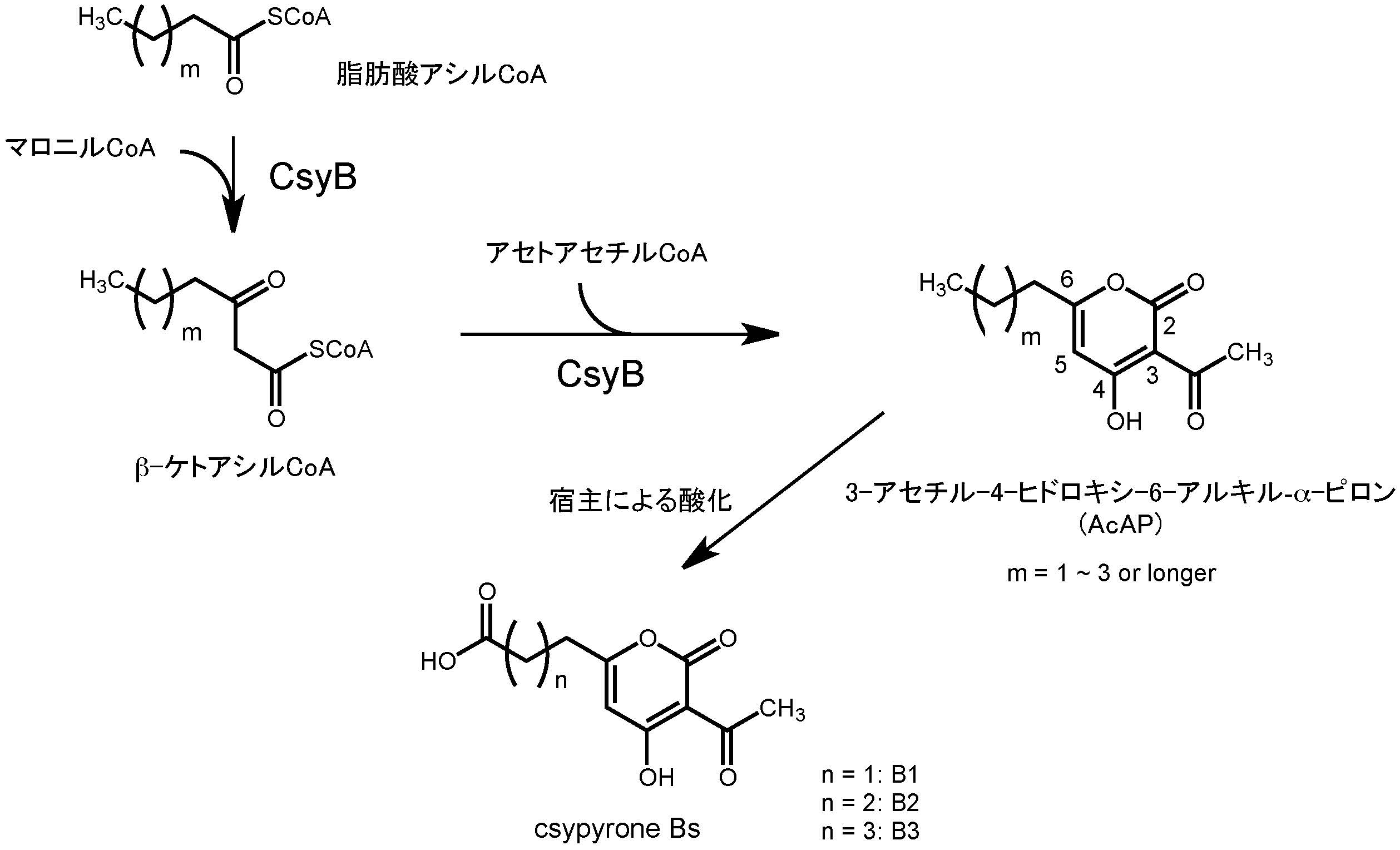
図 csypyrone B類の生合成とCsyBによるAcAPの生成(拡大画像↗)
タイプIII型PKSはカルコンやスチルベン、クルクミンなど多彩な骨格および生理活性をもつ化合物の生成に関与する酵素であり、植物由来のものについては数多く報告されています。また、比較的小さいタンパクであることから、その機能を利用した有用物質生産への応用が進められています。一方、糸状菌由来のIII型PKSは、麹菌ゲノムから4種類のIII型PKS遺伝子が初めて見出されて以来、複数の菌でその存在が確認されていますが、機能まで詳細に解析された例は多くありません。
同研究グループは、麹菌由来のcsyB遺伝子を同種の麹菌を宿主として誘導発現し、3-アセチル-4-ヒドロキシ-α-ピロン骨格に脂肪酸が付加した新規化合物csypyrone B 類が生産されることを確認していました。また、csyB誘導発現株への標識酢酸投与実験の結果から、CsyBが脂肪酸アシルCoAとマロニルCoA、アセトアセチルCoA(もしくはアセトマロニルCoA)からAcAPを生成した後、宿主内で酸化されてcsypyrone Bへ変換されるものと予想していました。そこで、これを実証するため、今回、大腸菌での発現、および組換え酵素を用いてCsyBの機能解析を行いました。
はじめにcsyB遺伝子を導入した大腸菌を培養したところ、その培養液中に、遺伝子特異的に生産される複数の化合物を確認しました。核磁気共鳴装置(NMR)等の解析から、これら生成物は6位にC9~C17のアルキル鎖もしくはアルケニル鎖をもつAcAPであることを明らかにしました。このことからCsyBが上記の反応を触媒することが強く示唆されました。
次に大腸菌内で発現させたCsyBとTF(注3)との融合タンパク(TF-CsyB)をアフィニティーカラム精製(注4)し、この組換え酵素を用いて試験管内での活性試験を行いました。ブチリルCoA(鎖長C4)を開始基質に、マロニルCoAとアセトアセチルCoAを伸長基質として反応させたところ、酵素特異的に生成する2つのピークを検出しました。そのうちの1つは化合物のUV吸収および質量分析から6位にプロピル基をもつAcAPでした。さらに開始基質をC6~C18の脂肪酸アシルCoAとして同様の活性試験を行ったところ、C6~C10の脂肪酸アシルCoAを用いた時にC5~C9の側鎖をもつAcAPが生成することを確認しました。また、各反応で2分子のアセトアセチルCoAが縮合したデヒドロ酢酸の生成も同時に検出されました。つまり、CsyBは開始基質である脂肪酸アシルCoAとマロニルCoAとの反応よりβ-ケトアシルCoAを生成するとともに、もう一分子のβ-ケトアシルCoA(アセトアセチルCoA)を縮合させてAcAPを生成することが明らかになりました。さらに2分子のβ-ケトアシルCoA縮合活性を確認するため、β-ケトヘキサン酸誘導体を化学的に調製し、CsyBと反応させたところ、予想した3-ブチリル-4-ヒドロキシ-6-プロピル-α-ピロンが生成することを確認しました。
以上の結果から、研究グループはCsyBが2分子β-ケトアシルCoAの縮合反応を触媒できる新規タイプIII型PKSであることを実証しました。このような活性を有するIII型PKSはCsyBが初めての例であり、C4~C18のアルキル鎖(もしくはアルケニル鎖)をもつ脂肪酸アシルCoAが開始基質となり得ることから、マロニルCoAとの反応後に縮合に関与するもう一つのβ-ケトアシルCoAと組み合わせることで、多様なAcAP化合物の生成が可能になるものと考えられます。また、関連化合物にHIVインテグラーゼ阻害活性(注5)などが報告されており、CsyBが生成できるAcAP化合物の生理活性にも興味が持たれます。
発表雑誌
- 雑誌名
- 「The Journal of Biological Chemistry」(7月18日号)
- 論文タイトル
- Aspergillus oryzae CsyB catalyzes the condensation of two β-ketoacyl-CoAs to form 3-acetyl-4-hydroxy-6-alkyl-α-pyrone
- 著者
- Makoto Hashimoto1, Tsukasa Koen1, Hiroaki Takahashi1 Chihiro Sudasu1, Katsuhiko Kitamoto2, and Isao Fujii1
1 岩手医科大学薬学部
2 東京大学大学院農学生命科学研究科 応用生命工学専攻 - DOI番号
- 10.1074/jbc.M114.569095
- アブストラクト
- http://www.jbc.org/content/289/29/19976
問い合わせ先
東京大学大学院農学生命科学研究科 応用生命工学専攻 微生物学研究室
教授 北本 勝ひこ(キタモトカツヒコ)
Tel:03-5841-5161
Fax:03-5841-8033
研究室URL:http://park.itc.u-tokyo.ac.jp/Lab_Microbiology/hyousi.html
岩手医科大学薬学部 天然物化学講座
教授 藤井 勲(フジイイサオ)
〒028-3694 岩手県紫波郡矢巾町西徳田2-1-1
Tel:019-651-5110 ext. 5260
Fax:019-698-1923
研究室URL:http://inpc.iwate-med.ac.jp
用語解説
- 注1 麹菌
- 麹菌Aspergillus oryzaeは味噌や醤油、日本酒などの製造に古くから利用されている糸状菌。
- 注2 PKS:ポリケタイド合成酵素(polyketide synthase)
- 単純な脂肪酸誘導体を縮合して多彩な構造と生理活性をもつポリケタイド化合物を生成する酵素。構造上の違いからI~III型に分類され、糸状菌がもつPKSの多くは巨大な1つのタンパクにドメイン(構成するタンパク質の内、反応を触媒するために重要な領域)が複数存在するI型に分類される。III型は縮合酵素ドメインのみからなり、植物のカルコン合成酵素などが含まれる。
- 注3 TF:トリガーファクター(trigger factor)
- 大腸菌のシャペロンタンパクの一種で、発現タンパクの正常な折りたたみや可溶化に関与する。
- 注4 アフィニティーカラム精製
- 目的タンパク質と親和性を持つ低分子化合物や抗体をカラム充填剤の表面に結合させておき、目的タンパク質を含む試料を通過させることで親和性のないタンパク質を除去し、その後、目的タンパク質を溶出させることで他の成分と分ける精製方法。
- 注5 HIVインテグラーゼ阻害活性
- ヒト免疫不全ウイルス(HIV)は、はじめに宿主(ヒト)の免疫細胞内に侵入後、逆転写酵素によって遺伝情報をRNAからDNAに変換する。その後、インテグラーゼによってウイルスDNAの一部が宿主細胞DNA内に取り込まれ、ウイルスが複製することで感染が成立する。そのため、インテグラーゼ阻害活性を有する化合物は、ウイルスDNAの宿主細胞DNAへの取り込みを防ぎ、ウイルス複製をさせないようにすることから、HIV治療薬として期待されている。