酵母による異宿主タンパク質発現系における新規ランダム変異導入法の開発
- 発表者
-
立岡 美夏子(東京大学大学院農学生命科学研究科 生物材料科学専攻 博士課程学生 日本学術振興会特別研究員)
杉本 直久(東京大学大学院農学生命科学研究科 生物材料科学専攻 農学特定研究員(当時))
中村 彰彦(東京大学大学院農学生命科学研究科 生物材料科学専攻 博士課程学生 日本学術振興会特別研究員(当時))
砂川 直樹(東京大学大学院農学生命科学研究科 生物材料科学専攻 農学特定研究員)
石田 卓也(東京大学大学院農学生命科学研究科 生物材料科学専攻 特任助教)
内山 拓(東京大学大学院農学生命科学研究科 生物材料科学専攻 農学特定研究員)
五十嵐 圭日子(東京大学大学院農学生命科学研究科 生物材料科学専攻 准教授)
鮫島 正浩(東京大学大学院農学生命科学研究科 生物材料科学専攻 教授)
発表のポイント
◆異宿主タンパク質の生産性の高さで知られるピキア酵母において、簡便なランダム変異導入法の開発に成功しました。
◆2段階のDNA増幅法を組み合わせることにより、ピキア酵母おけるトランスフォーメーション効率の低さを補い、ランダムに変異させたDNAをピキア酵母に直接導入できるようになりました。
◆大腸菌などで発現が難しい真核生物由来のタンパク質などの機能解析に、大きく貢献できることが期待されます。
発表概要
大学院農学生命科学研究科生物材料科学専攻の立岡美夏子学術振興会特別研究員、五十嵐圭日子(きよひこ)准教授および鮫島正浩教授らのグループは、異宿主タンパク質の高生産性で知られるメタノール資化性酵母Pichia pastoris(ピキア酵母)注1において、簡便にランダム変異導入注2ができる実験系の開発に成功しました。ピキア酵母への遺伝子導入は、一般的な大腸菌の遺伝子組換えに用いられる100万倍量程度のDNAが必要であるため、ランダム変異導入には不向きであると考えられてきました。そこでグループは、1段階目として枯草菌ファージφ29が生産するDNAポリメラーゼ(φ29DNAポリメラーゼ)注3をマンガンイオン存在下で反応させてランダムに変異を導入し、さらに変異が入ったDNAに対してマンガンイオンを含まない条件でφ29DNAポリメラーゼによって増幅させることで、本酵母への遺伝子導入に十分な変異導入DNAを簡便に調製しました。セルロース系バイオマスの変換に重要なセルラーゼ(PcCel6A)遺伝子に対して本手法を適用したところ、平均して1000塩基当たり2.6塩基に変異が導入されており、一般的なランダム変異導入率(1000塩基当たり約3塩基)とほぼ同じ変異導入率であることが分かりました。本手法の開発によって、大腸菌で生産することが難しい様々なタンパク質に対してもランダム変異導入を用いた解析が可能となります。
発表内容
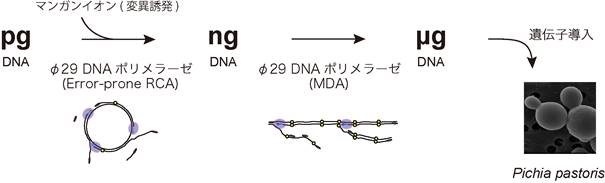
図1 ランダム変異導入法の概要。φ29DNAポリメラーゼを用いた2ステップの手法でマイクログラム(µg)量のDNAを増幅する。(拡大画像↗)
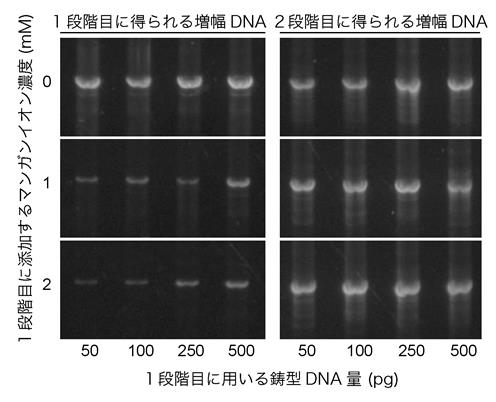
図2 1段階目および2段階目に得られる増幅DNA量。変異誘発にマンガンイオンを使用した際も、2段階増幅後には十分量のDNAが得られる。(拡大画像↗)
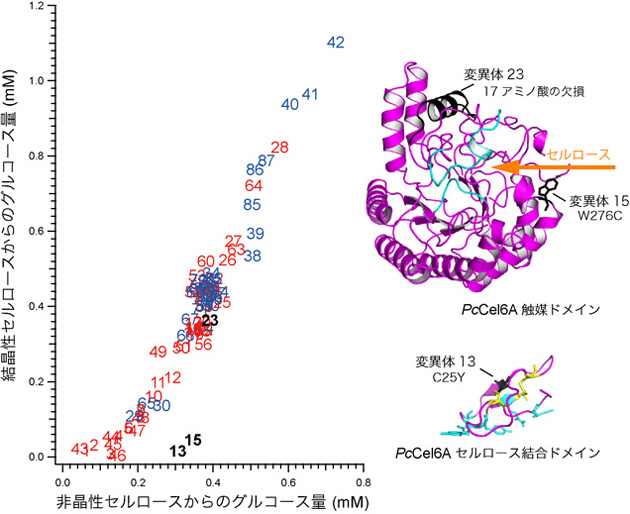
図3 変異PcCel6Aの活性測定結果およびその変異導入箇所の一部結果。グラフ赤字:変異PcCel6A 青字:コントロール(変異導入されていないPcCel6A)(拡大画像↗)
1990年代のバイオテクノロジーの進展によって、タンパク質を人工的に生産することが可能となり、現在では医療、食品・繊維加工、発酵、バイオマス変換など様々な分野にその技術が利用されています。それらのタンパク質を構成するアミノ酸を人為的に変化させることで、タンパク質としての性状を変えたり酵素としての反応性を向上させることを変異導入と呼びますが、これには大きく分けて2つの方法が知られています。1つは論理的変異導入法と呼ばれるもので、これまでに集められた様々なタンパク質のアミノ酸配列情報や三次元構造情報をもとに、変異させる箇所と目的のアミノ酸を定めて変異を導入する手法です。タンパク質に関する情報はすでに20世紀後半から様々なデータベースに蓄えられているため、最近ではかなり効率良く論理的変異を導入する箇所(アミノ酸)の特定ができるようになりました。しかしながら、現在の技術ではアミノ酸を変異させて得られるタンパク質がどのような性質を持ち得るのかを完全に推測することは難しいため、このような研究はトライ・アンド・エラーで進めているのが実情です。その一方で、偶発的にDNAに変異を導入し、アミノ酸を論理的ではなく無作為に変化させる手法がランダム変異導入法と呼ばれる手法です。この手法では、あえて使用するDNAポリメラーゼがミスをする条件を使用してDNAを増幅させることで、遺伝子の様々な箇所に変異を導入し、その結果アミノ酸をランダムに変化させることができます。この手法によって得られる変異タンパク質は、これまでに蓄積された情報からは予想ができないような性質を持つ可能性があるため、論理的な変異導入と平行して行うことで新しい機能を持つタンパク質を作成できるようになります。
このような異宿主タンパク質の生産には、細菌や酵母、糸状菌、植物細胞、昆虫細胞、動物細胞など様々な宿主が用いられますが、その中でもメタノール資化性酵母の一種であるPichia pastoris(ピキア酵母)は、タンパク質生産能が極めて高く、しかもタンパク質生産に古くから用いられてきた大腸菌では生産が難しいとされる真核生物由来のタンパク質も生産できることから、すでに様々なタンパク質の異宿主生産系が構築されております。しかしながら、大腸菌の場合はピコグラム(pg、1グラムの1兆分の1の重さ)程度のDNA量で十分遺伝子導入ができるのに対して、ピキア酵母はDNAの導入率が極めて低く、マイクログラム(μg、1グラムの100万分の1)、すなわち大腸菌の場合の100万倍のDNA量を用いないと遺伝子導入ができないという難点があります。変異を導入していないDNAや論理的変異を導入したDNAの場合は、大腸菌で目的のDNAを増幅した後にピキア酵母に遺伝子導入をすれば良いのですが、ランダム変異導入の場合は、いかにランダムに変異の入ったDNAをバイアスをかけずにマイクログラムレベルまで増幅し、ピキア酵母に遺伝子導入するかが課題でした。
本研究では枯草菌ファージの一種であるφ29が生産するDNAポリメラーゼが、一定温度でDNAを増幅し、さらに金属イオン存在下で増幅ミスをするという性質を利用して、マンガンイオン有り(一段目: Error-prone Rolling Circle Amplification, error-prone RCA)と無し(二段目:Multiple Displacement Amplification, MDA)の2段階のφ29DNAポリメラーゼ増幅によって、簡便に数マイクログラムのランダム変異導入DNAを調製し、ピキア酵母にそのDNAを導入することに成功しました(図1、図2)。この手法を、担子菌(きのこ)の一種であるPhanerochaete chrysosporiumがセルロースを分解する際に分泌し、高効率でセルロース系バイオマスの糖化をすることができるセルラーゼPcCel6Aへの変異導入に用いたところ、100種類程度の変異酵素を生産するピキア酵母を得ることができました。この実験で得られたピキア酵母によって生産された様々な変異PcCel6Aの活性を調べたところ、酵素分解されにくい結晶性を有するセルロースを分解するために重要なアミノ酸の箇所や、タンパク質の一部(ドメイン)に関する情報を得ることができました(図3)。
本研究では、セルロース系バイオマスを効率良く分解できる変異酵素を探索することを目的として手法開発を行いましたが、これまで一般的に用いられてきたポリメラーゼ連鎖反応(PCR)注4と大腸菌を組み合わせる手法と比較して本手法は非常に簡便であるため、ピキア酵母によるランダム変異タンパク質の生産に広く用いられることが期待されます。さらに本研究で用いた二段階DNA増幅法によって、ランダム変異導入したDNAを大量に調製できることが証明されたことから、ピキア酵母だけでなく様々な宿主にも応用が可能で、タンパク質の機能解析がさらに加速することが期待されます。
本研究は、新エネルギー・産業技術総合開発機構(NEDO)「セルロース系エタノール革新的生産システム開発事業」(鮫島正浩)、科学技術振興機構(JST)革新的研究開発推進プログラム(ImPACT)「豊かで安全な社会と新しいバイオものづくりを実現する人工細胞リアクタ」(プログラムマネージャー:東京大学 野地博行 教授、研究分担者:五十嵐圭日子)、文部科学省科学研究費補助金新学術領域研究「植物細胞壁の情報処理システム」(領域代表:東北大学 西谷和彦 教授、計画研究代表者:五十嵐圭日子)、日本学術振興会科学研究費補助金(五十嵐圭日子)、日本学術振興会特別研究員奨励費(立岡美夏子)および旭硝子財団助成研究(五十嵐圭日子)からの補助を受けたものです。
発表雑誌
- 雑誌名
- 「Biotechnology for Biofuels」
- 論文タイトル
- Development of simple random mutagenesis protocol for the protein expression system in Pichia pastoris
- 著者
- Mikako Tachioka(立岡美夏子)、Naohisa Sugimoto(杉本直久)、Akihiko Nakamura(中村彰彦)、Naoki Sunagawa(砂川直樹)、Takuya Ishida(石田卓也)、Taku Uchiyama(内山拓)、Kiyohiko Igarashi(五十嵐圭日子)、Masahiro Samejima(鮫島正浩)
- DOI番号
- 10.1186/s13068-016-0613-z
- 論文URL
- http://biotechnologyforbiofuels.biomedcentral.com/articles/10.1186/s13068-016-0613-z
問い合わせ先
東京大学大学院農学生命科学研究科 生物材料科学専攻 森林化学研究室
教授 鮫島正浩(さめじま まさひろ)
Tel:03-5841-5255
Fax:03-5841-5273
E-mail:amsam@mail.ecc.u-tokyo.ac.jp
准教授 五十嵐 圭日子(いがらし きよひこ)
Tel:03-5841-5258
Fax:03-5841-5273
E-mail:aquarius@mail.ecc.u-tokyo.ac.jp
用語解説
- 注1 メタノール資化性酵母Pichia pastoris(ピキア酵母)
- 炭素源・エネルギー源としてメタノールを利用できる酵母の一種で、非常に高い菌体密度で培養できるという特徴があるため、タンパク質の大量生産によく用いられる。目的のタンパク質を菌体外に生産するための遺伝子操作法も確立されている。
- 注2 ランダム変異導入
- DNA を構成する塩基に置換、挿入、欠損などの配列の変化を生じさせる技術。その際に特定の遺伝子変化をねらうのではなく敢えてできる限り異なった遺伝子を作り出すことで、得られるタンパク質に多様性を持たせることができる。
- 注3 φ29DNAポリメラーゼ
- 2本鎖DNAを1本鎖にほどきながらDNA合成を進めることができる鎖置換活性を持つDNA合成酵素(ポリメラーゼ)。特定のプライマーを設計することなく指数関数的にDNAを増幅できるため、環状DNA やゲノムDNAの増幅などに用いられている。
- 注4 ポリメラーゼ連鎖反応(PCR)
- ポリメラーゼによるDNA合成反応の際に反応温度を変化させることによってDNAの 2本鎖形成を制御し、鋳型DNAから2つのプライマーではさまれた領域のDNAを増幅する手法。