東京大学大学院 農学生命科学研究科 研究成果
変異を導入した担子菌由来β-1,3/1,6-グルカナーゼLam16Aを用いた環状βグルカンの人工合成
- 発表者
- Jonas Vasur (スウェーデン農業科学大学・博士課程学生)
川合 理恵 (東京大学・大学院農学生命科学研究科・学術振興会特別研究員)
K. Hanna M. Jonsson (ストックホルム大学・博士課程学生)
Göran Widmalm (ストックホルム大学・講師)
Åke Engström (ウプサラ大学・主任研究員)
Martin Frank (ドイツ癌研究センター・アシスタントコーディネーター)
Evalena Andersson (スウェーデン農業科学大学・博士研究員)
Henrik Hansson (スウェーデン農業科学大学・助教)
Zarah Forsberg (ウプサラ大学・修士課程学生)
五十嵐 圭日子 (東京大学・大学院農学生命科学研究科・准教授)
鮫島 正浩 (東京大学・大学院農学生命科学研究科・教授)
Mats Sandgren (スウェーデン農業科学大学・講師)
Jerry Ståhlberg (スウェーデン農業科学大学・准教授)
発表概要
スウェーデン農業科学大学と東京大学は、活性アミノ酸残基に変異を導入した担子菌由来β-1,3/1,6-グルカナーゼ(Lam16A)の結晶構造中で、ラミナリヘプタオースが環状構造を取っていることを発見しました。さらに、還元末端をフッ素化したラミナリヘプタオース(フッ化ラミナリヘプタオース)を本変異酵素とインキュベートし、還元末端と非還元末端がβ-1,3-グルコシド結合した環状βグルカンの人工合成に世界で初めて成功しました。
発表内容
糸状菌は細胞壁成分としてβ-1,3/1,6-グルカン注1を生成しますが、この成分はヒト体内では難消化性で抗腫瘍作用などの生理活性を有することが報告されています。一方糸状菌は、成長の様々なステージでラミナリナーゼと呼ばれるβ-1,3-グルカンの加水分解酵素を生産し、細胞壁量をコントロールしたり、構造を変化させたりすることが知られています。担子菌Phanerochaete chrysosporiumが生産するβ-1,3/1,6-グルカナーゼLam16Aは、糖質加水分解酵素ファミリー16に属し、エンド型にβグルカン分解することが知られております。これまで、東京大学はスウェーデン農業科学大学との共同研究で、本酵素の結晶構造解析に取り組み、さらにオリゴ糖を活性中心に取り込んだ結晶構造に関しても長年解析を進めてきました参考論文1、2。
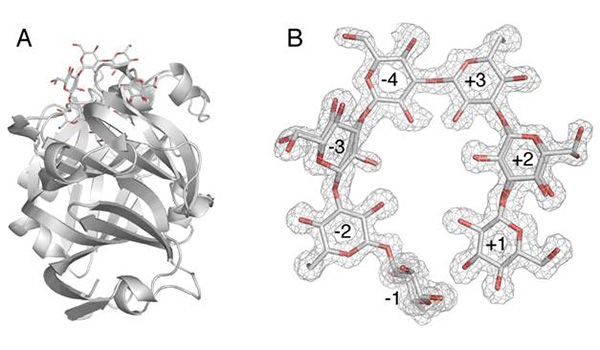
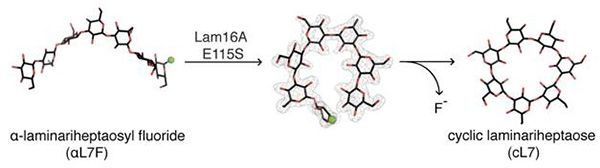
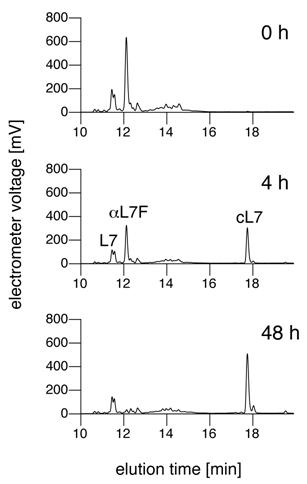
本研究では、活性アミノ酸残基である115番目のグルタミン酸をセリンにした変異酵素(E115S)の結晶構造を、ラミナリヘプタオースが活性中心に結合した状態で解き、本基質が活性中心を挟んで環状になって酵素に取り込まれていることを発見しました(図1)。さらに、還元末端をフッ素化したラミナリヘプタオース(フッ化ラミナリヘプタオース:αL7F)を本変異酵素とインキュベートすることで、ラミナリヘプタオース分子中の還元末端が非還元末端と共有結合した環状ラミナリヘプタオース(cL7)が生成することが明らかとなりました(図2、図3)
自然界では、ある種の細菌が抗生物質として微量の環状β-1,3-グルカンを生産するという報告はありましたが、これまでに環状βグルカンの人工合成に成功した例はありません。また、環状オリゴ糖として広く知られているシクロデキストリン注2の場合は、空孔内部が疎水性であるのに対して、本研究で合成された環状β-1,3-グルカンの場合は空孔内部が親水性であると考えられることから、シクロデキストリンとは全く性質の異なる難消化性の包摂化合物としての利用が期待されます。
本研究は東京大学大学院農学生命科学研究科とスウェーデン農業科学大学との学術協定をもとに行われた共同研究の成果です。
参考論文
1 Jonas Vasur, Rie Kawai, Anna M. Larsson, Kiyohiko Igarashi, Mats Sandgren, Masahiro Samejima and Jerry Ståhlberg
X-ray crystallographic native sulfur SAD structure determination of laminarinase Lam16A from Phanerochaete chrysosporium
Acta crystallographica. Section D, Biological crystallography 62:1422-1429 (2006)
2 Jonas Vasur, Rie Kawai, Evalena Andersson, Kiyohiko Igarashi, Mats Sandgren, Masahiro Samejima and Jerry Ståhlberg
X-ray crystal structures of Phanerochaete chrysosporium Laminarinase 16A in complex with products from lichenin and laminarin hydrolysis
FEBS Journal 276:3858-3869 (2009)
発表雑誌
Synthesis of Cyclic β-Glucan Using Laminarinase 16A Glycosynthase Mutant from the Basidiomycete Phanerochaete chrysosporium
Jonas Vasur, Rie Kawai, K. Hanna M. Jonsson, Göran Widmalm, Åke Engström, Martin Frank, Evalena Andersson, Henrik Hansson, Zarah Forsberg, Kiyohiko Igarashi, Masahiro Samejima, Mats Sandgren and Jerry Ståhlberg
問い合わせ先
東京大学・大学院農学生命科学研究科・生物材料科学専攻・森林化学研究室
〒113-8657 東京都文京区弥生1-1-1
Tel: 03-5841-5255
Fax: 03-5841-5273
E-mail: amsam@mail.ecc.u-tokyo.ac.jp
森林化学研究室ホームページ
URL: http://web2.fp.a.u-tokyo.ac.jp/lab-forechem.html
用語解説
糸状菌細胞壁の主成分で、β-1,6-グルカンの分岐を有するβ-1,3-グルカン。一般的にβグルカンと呼ばれている多糖
注2 シクロデキストリン:α-1,4-グルカンオリゴ糖の還元末端と非還元末端が結合して環状構造をとった化合物。環状構造の内部は疎水性で、小さな分子を包接できることが知られている。