東京大学大学院 農学生命科学研究科 プレスリリース
アミノ酸配列からタンパク質の機能を予測できない場合においても、立体構造情報を利用してその機能を解明することが可能である。
- 発表者
- 田之倉 優 (東京大学大学院農学生命科学研究科 応用生命化学専攻 教授)
永田 宏次 (東京大学大学院農学生命科学研究科 応用生命化学専攻 准教授)
宮川 拓也 (東京大学大学院農学生命科学研究科 応用生命化学専攻 特任助教)
堀田 彰一朗 (東京大学大学院農学生命科学研究科 応用生命化学専攻 博士課程2年)
山川 稔 ((独)農業生物資源研究所 昆虫科学研究領域 特任上級研究員、筑波大学大学院生命環境科学研究科 教授)
石橋 純 ((独)農業生物資源研究所 昆虫科学研究領域 生体防御研究ユニット長)
発表概要
既知のタンパク質とアミノ酸配列の類似性がまったくないタンパク質オリクチンの分子の立体構造を決定し、立体構造の類似性から機能を明らかにしました。タンパク質の立体構造解析が機能解明のために有効な手法であることを示しました。
発表内容
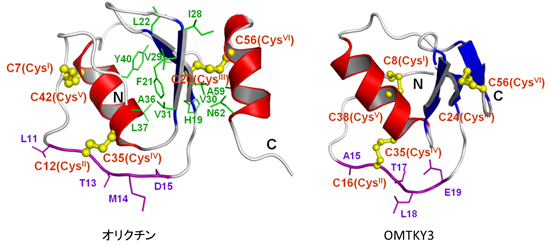
図1. タイワンカブトムシ由来オリクチンのNMR構造(左)と七面鳥由来OMTKY3のX線結晶構造(右)。オリクチンのC末側へリックス(右側のへリックス)以外の領域とOMTKY3の間に立体構造の類似性があることが示された。
オリクチンはタイワンカブトムシ(Oryctes rhinoceros)の体液中から見つかった66アミノ酸残基からなるタンパク質で、他のタンパク質・ペプチドに対してアミノ酸配列の類似性が見出せないため、どのような機能を有するタンパク質か知る手がかりがありませんでした。
ゲノム研究などの進展により、数多くのタンパク質が新たに見つかっていますが、新規タンパク質の約5%はオリクチンのように他のタンパク質とのアミノ酸配列の相同性が極めて低いため、機能予測が困難であり、このことが生物学の発展を妨げる一因になっています。
我々はアミノ酸配列ではなく、分子の立体構造の類似性から、オリクチンの機能解明に迫れないかと考え、タンパク質分子の立体構造決定法の一つである多次元核磁気共鳴(NMR)法を用いて、オリクチン分子の立体構造を決定しました。立体構造が類似しているタンパク質を立体構造データベース(Protein Data Bank)で検索したところ、アミノ酸配列の相同性が極めて低いにもかかわらず、七面鳥のセリンプロテアーゼ(タンパク質分解酵素)阻害剤の一種、オボムコイドインヒビター(OMTKY3)(注1)と分子の立体構造が似ていることが明らかになりました(図1)。類似性に基づいて活性試験を行い、オリクチンが実際にOMTKY3と同様、セリンプロテアーゼ阻害剤として機能することを明らかにしました。ただし、すべてのセリンプロテアーゼを阻害するのではなく、真核生物由来のキモトリプシン様セリンプロテアーゼと細菌由来のズブチリシン様セリンプロテアーゼに対し強い阻害活性を示しました。この結果から、オリクチンがタイワンカブトムシの体内で、感染防御の役割を担っていることが示唆されました。
このように本研究では、タンパク質分子の立体構造に基づいて、その機能を解明することに成功しました。
近年、ゲノムDNAの塩基配列が次々に解読されておりますが、全体の約5%のタンパク質については、機能既知のタンパク質やその機能単位(ドメイン、モチーフ)との間にアミノ酸配列の相同性がなく、機能の推定すらできないままとなっています。それらの一部は、遺伝子ノックアウト、ノックダウン、過剰発現、相互作用解析等の手法により機能の同定が進められています。本研究の成果は、それらの技術に加え、他のタンパク質とアミノ酸配列の類似性を持たない機能未知のタンパク質であっても、立体構造情報から機能を特定できることを実証しており、タンパク質の立体構造解析が、今後の分子生物学の発展に大きく寄与する可能性を示しています。
共同研究・助成など:本研究は文部科学省ターゲットタンパク研究プログラムおよび科学技術振興調整費COE育成プログラムにより支援を受けております。
発表雑誌
(2010年7月14日電子版掲載, 2010年9月24日刊行)
Isolation, cDNA cloning, and structure-based functional characterization of oryctin, a hemolymph protein from the coconut rhinoceros beetle, Oryctes rhinoceros, as a novel serine protease inhibitor.
Horita, S., Ishibashi, J., Nagata, K., Miyakawa, T., Yamakawa, M. and Tanokura, M.
問い合わせ先
応用生命化学専攻
教授 田之倉 優
Tel: 03-5841-5165
FAX: 03-5841-8023
E-mail: amtanok@mail.ecc.u-tokyo.ac.jp
用語解説
the third domain of turkey ovomucoid inhibitorの意。OMKTY3は七面鳥の卵白に含まれる糖タンパク質であり、3つの繰り返し単位からなる。各単位がタンパク質分解酵素の阻害剤として働き、細菌等が分泌するタンパク質分解酵素の活性を阻害し、外敵から身を守るための生体防御に関与していると考えられている。