東京大学 農学生命科学研究科 研究成果
ロイシンによるグルタミン酸脱水素酵素のアロステリック制御機構の解明
- 発表者
- 富田 武郎 (東京大学生物生産工学研究センター・助教)
葛山 智久 (東京大学生物生産工学研究センター・准教授)
西山 真 (東京大学生物生産工学研究センター・教授)
発表概要
好熱菌(注1)の炭素・窒素代謝を連結する酵素であるグルタミン酸脱水素酵素(GDH)とロイシンとの複合体の立体構造を明らかにし、アロステリック制御(注2)機構を解明した。また、ロイシンによるアロステリック制御機構がヒトなど哺乳類由来GDHと共通している可能性を示した。本研究成果は、ロイシンの生体調節因子としての機能の解明につながるものと期待される。
発表内容
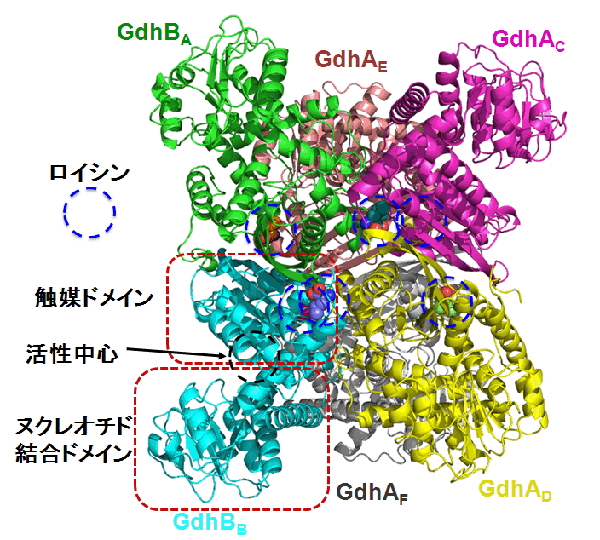
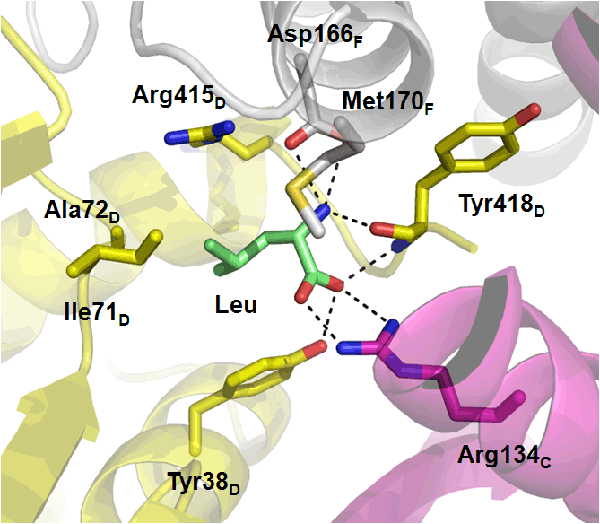
GDHは、α-ケトグルタル酸とグルタミン酸との間の可逆的変換を触媒する酵素である。炭素・窒素代謝を連結する代謝の中枢を担うために、ほとんどの生物がこの酵素を有している。好熱菌Thermus thermophilus由来GDHはロイシンによって強く活性化を受けるという特徴を有する。東京大学生物生産工学研究センターの富田助教、西山教授らは、T. thermophilusのGDHとロイシンとの複合体の結晶構造を、大学共同利用機関法人高エネルギー加速器研究機構の物質構造科学研究所放射光科学研究施設を用いて明らかにした。一般に、GDHは同一サブユニット6個からなるホモ6量体を形成することが知られているが、決定した構造は、互いに相同性を有するGdhA(制御サブユニット)4つとGdhB(触媒サブユニット)2つから構成されるヘテロ6量体であり、GDHとしては初めてのヘテロ6量体の構造となった(図1)。それらサブユニット間の境界領域に存在するポケットにロイシンが結合していることを見出し、同部位へのロイシンの結合がGDHの活性化を引き起こすことを明らかにした(図2)。
一方、ヒトやウシのGDHもロイシンによって活性化されることが知られているが、その機構は不明なままであった。アミノ酸配列を比較したところ、T. thermophilusのGDHにおいてロイシン結合に関わるアミノ酸残基がヒトやウシのGDHにも保存されており、哺乳類のGDHもまた同様な機構でロイシンによって活性化される可能性が考えられた。そこで、保存アミノ酸をロイシンが結合できなくなるように置換したヒトGDH2の変異酵素を作製し、ロイシンに対する感受性の変化を調べたところ、各変異体はロイシンによる活性化能を消失していることがわかった。この結果は、栄養シグナルとして機能するロイシンのセンシング機構の一端を明らかにしただけでなく、哺乳類のGDHの活性化についても重要な情報を提示することになった。哺乳類のGDHは複雑に制御され、GDH活性の脱制御を与える変異の幾つかは高インスリン症/高アンモニア血症(注3)の原因と同定されている。本研究の成果は、GDHをターゲットとした創薬開発にもつながるものと期待される。