切るメカニズムが違った!特定の配列を認識しDNAを切断する酵素の新しい仕組みを発見
- 発表者
-
宮園 健一(東京大学大学院農学生命科学研究科 応用生命化学専攻 特任助教)
古田 芳一(東京大学大学院新領域創成科学研究科 メディカルゲノム専攻 特任助教)
渡部(松井) 美紀(東京大学大学院新領域創成科学研究科 メディカルゲノム専攻 博士課程3年;当時)
宮川 拓也(東京大学大学院農学生命科学研究科 応用生命化学専攻 助教)
伊藤 友子(東京大学大学院農学生命科学研究科 応用生命化学専攻 特任研究員)
小林 一三(東京大学大学院新領域創成科学研究科 メディカルゲノム専攻 教授)
田之倉 優(東京大学大学院農学生命科学研究科 応用生命化学専攻 教授)
発表のポイント
◆DNAの塩基配列を操作する遺伝子組み換え技術に欠かせない制限酵素の新しい働きを古細菌の一種で発見しました。
◆DNA塩基配列中の糖と塩基の間の結合を切断する(DNAグリコシラーゼ活性)制限酵素を世界に先駆けて発見しました。
◆本成果は、細菌のもつ特定な塩基配列を認識しDNAを分解する機構について、これまでの常識を覆すもので、今後も、同種の酵素が発見されると期待されます。
発表概要
DNAの塩基配列を操作する遺伝子組み換えは、薬の大量生産や正常な遺伝子を患者さんに補充する遺伝子治療などで利用されている技術です。この技術には、特定の塩基配列を認識して二本鎖のDNAを切断する酵素群(制限酵素)は欠かせません。DNAは、塩基に糖とリン酸が結合し直鎖状に連なった構造を持ち、これまで制限酵素は、糖とリン酸の間の結合(ホスホジエステル結合)を切断する(エンドヌクレアーゼ活性)と考えられてきました。
今回、東京大学大学院農学生命科学研究科の田之倉優教授を中心とする研究グループは、X線結晶構造解析法(注1)とさまざまな分析手法を組み合わせることにより、超好熱古細菌Pyrococcus abyssi(注2)由来の制限酵素R.PabIは、DNA塩基配列中の糖と塩基の間の結合を切断する(DNAグリコシラーゼ活性)酵素であることを見出しました。R.PabIは認識した塩基配列中のアデニンと呼ばれる塩基と糖の切断を触媒し脱塩基部位(注3)を生み出します。R.PabIの触媒反応によって生じた脱塩基部位は、熱分解もしくは他の酵素の作用によって切断され、最終的には二本鎖のDNAがバラバラになります。
DNAグリコシラーゼ活性をもつ制限酵素の発見は、本研究によるものが初めてで、今後も同種の酵素が発見される可能性が期待されます。また、本成果は細菌のもつ特定な塩基配列を認識しDNAを分解する機構について、これまでの常識を覆すものです。
本研究の内容は英国科学誌「Nature Communications」1月24日号に掲載されました。
発表内容
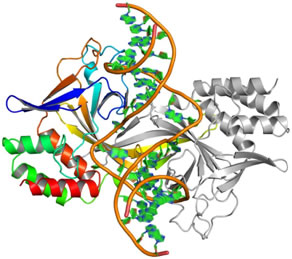
図1 X線結晶構造解析法により決定したR.PabI-DNA複合体構造
(拡大画像↗)
R.PabIは、二本鎖DNAを90°近く折り曲げてR.PabIと結合させます。R.PabIが認識する特定の配列(5’-GTAC-3’)は、折れ曲がりの頂点に位置します。
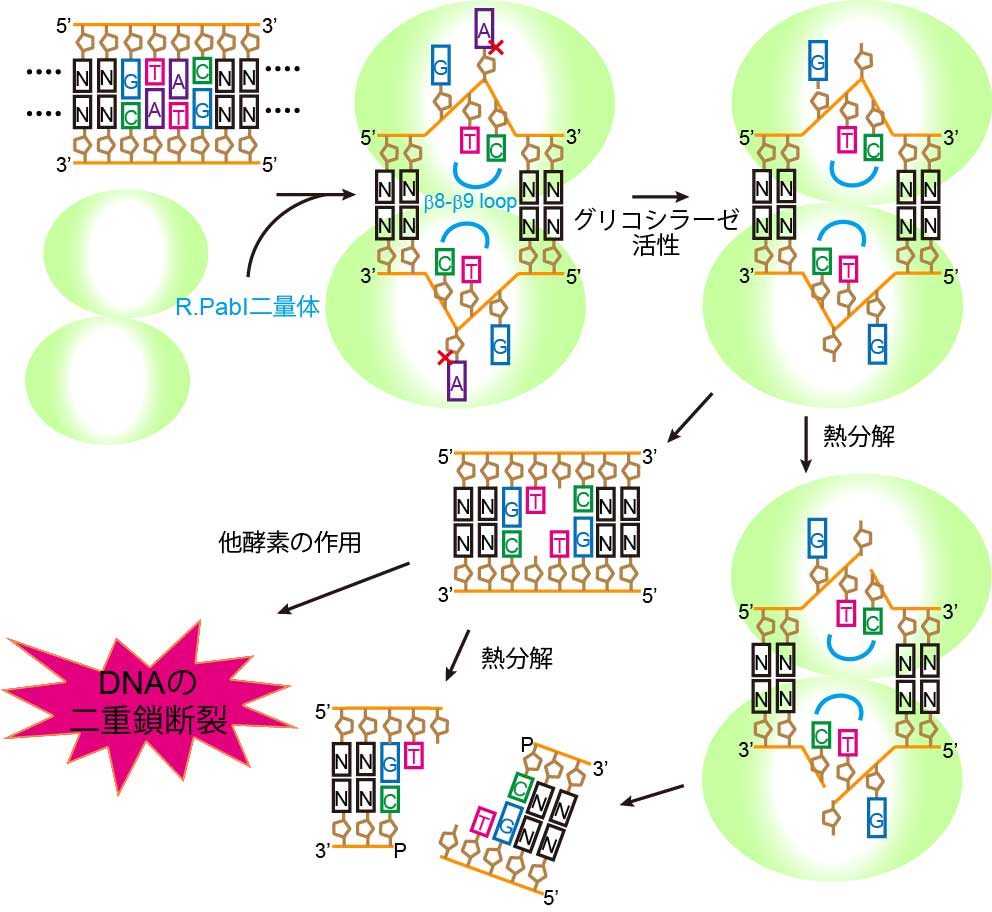
図2 R.PabIによるDNAの切断メカニズム(拡大画像↗)
R.PabIの触媒反応によって生じた向かい合った二つの脱塩基部位は、熱分解もしくは他の酵素の作用によって切断されます。
制限酵素とは、特定の塩基配列を認識して二本鎖DNAを切断する酵素群であり、細菌の外来DNAに対する自己防御機構として発見されました。このDNAを切断する機能はDNAの塩基配列を操作する遺伝子組み換えには欠かせないツールとなっており、制限酵素は遺伝子組み換え実験等に頻繁に利用されています。これまで制限酵素は、DNAのホスホジエステル結合を切断(加水分解)するエンドヌクレアーゼであると考えられてきました。
一方で超好熱古細菌Pyrococcus abyssi由来の制限酵素R.PabIは、東京大学大学院農学生命科学研究科の田之倉優教授らによって初めてその立体構造が決定され、特徴的な立体構造を取ることが知られていました。しかしながら、R.PabIがどのような機構でDNAを切断しているかに関しては不明なままでした。今回、東京大学大学院農学生命科学研究科の田之倉優教授を中心とする研究グループは、R.PabIによるDNAの切断機構を構造学的な手法により明らかにしようと試みました。
R.PabIとDNAの複合体(R.PabI-DNA複合体)の立体構造をX線結晶構造解析法により決定するため、R.PabIとR.PabIが認識する特定の配列(5’-GTAC-3’、認識配列)を含む二本鎖DNAの複合体の結晶を作製し、大型放射光施設(注3)Photon Factory AR-NE3AビームラインにてX線回折データを収集しました。得られたX線回折データを用いてR.PabI-DNA複合体の立体構造を決定したところ、1.R.PabIは二本鎖DNAを90°近く折り曲げてR.PabIと結合させること、2.R.PabIが配列を認識する部位では二本鎖DNAの向かい合った塩基間の相互作用が破壊されていることが明らかになりました(図1)。また、R.PabIが配列を認識する部位の付近の立体構造を精査したところ、認識配列中に含まれるアデニン塩基がDNA鎖から離れて存在していることが示唆されました。これは、R.PabIはエンドヌクレアーゼではなく、DNA中の塩基の脱離を触媒するDNAグリコシラーゼである可能性を示す結果です。これまでにDNAグリコシラーゼ活性をもつ制限酵素は一切知られていませんでしたが、R.PabIの触媒反応によって生じた産物を高速液体クロマトグラフィー(注4)やマトリックス支援レーザー脱離イオン化飛行時間型質量分析(注5)等で解析したところ、やはりR.PabIの添加によってアデニン塩基の脱離反応が引き起こされることが確認できました。またR.PabIの一部の構造に対し人工的に変異を導入したR.PabI変異タンパク質の解析を行うことにより、R.PabIによるDNAグリコシラーゼ反応を触媒する活性部位(注6)も同定しました。
以上の結果により、R.PabIは特定の配列を認識し、DNAグリコシラーゼ活性を示す制限酵素であることが明らかになりました。R.PabIの触媒反応によって、向かい合った二つの脱塩基部位をもつ二本鎖DNAが生み出されますが、このままでは向かい合った二つの脱塩基部位に結合が残っているため、二本鎖DNAの切断は引き起こされません。R.PabIの触媒反応によるアデニン塩基の脱離後に、熱による自然分解、もしくは他の酵素との共同的な作用が起こることによって、最終的に二本鎖DNAの切断がもたらされます(図2)。
R.PabIは既存のタンパク質とは立体構造が類似していない新奇性の高い酵素であり、特定の配列を認識し、DNAグリコシラーゼ活性を示す他に類を見ない反応を触媒します。R.PabIという酵素の存在が確認された今、R.PabIに類似した立体構造を持つ新規DNAグリコシラーゼや、エンドヌクレアーゼではない活性を示す他の新規な制限酵素等が発見される可能性が高まり、今後さまざまな研究へと発展する可能性が期待されます。
本研究は、文部科学省「タンパク3000プロジェクト」及び「ターゲットタンパク研究プログラム」の支援を受けて行われました。
発表雑誌
- 雑誌名
- 「Nature Communications」(オンライン版:1月24日)
- 論文タイトル
- A sequence-specific DNA glycosylase mediates restriction-modification in Pyrococcus abyssi
- 著者
- Ken-ichi Miyazono, Yoshikazu Furuta, Miki Watanabe-Matsui, Takuya Miyakawa, Tomoko Ito, Ichizo Kobayashi, and Masaru Tanokura
- DOI番号
- 10.1038/ncomms4178
- アブストラクト
- http://www.nature.com/ncomms/2014/140124/ncomms4178/abs/ncomms4178.html
問い合わせ先
東京大学大学院農学生命科学研究科 応用生命化学専攻 食品生物構造学研究室
教授 田之倉 優
Tel: 03-5841-5165
Fax: 03-5841-8023
研究室URL: http://fesb.ch.a.u-tokyo.ac.jp/
用語解説
- 注1 X線結晶構造解析法
- 生体高分子の結晶を作製しそこにX 線を照射すると、その結晶に特徴的な回折像を得られます。この回折像は、結晶を形成する分子の構造情報と相関するため、そのパターンや強度を解析することによって、目的分子の立体構造を決定することができます。
- 注2 超好熱古細菌
- 温泉や熱水域、強く発酵した堆肥、熱水噴出孔などの高温環境を好む古細菌で、80℃以上の環境で生育します。
- 注3 脱塩基部位
- DNA中のプリンおよびピリミジン塩基が欠失した部位を指します。脱塩基部位は構造的に不安定であり、早急に修復されないとDNAの切断が起こってしまいます。
- 注4 大型放射光施設
- タンパク質の立体構造解析の精度は、構造解析の際に用いるX 線回折データの品質(分解能)に大きく依存します。正確な立体構造を決定するためには、高品質・高強度なX 線を利用できる大型放射高施設の利用が必須です。
- 注5 高速液体クロマトグラフィー
- 機械的に高い圧力をかけることにより溶液を高流速で樹脂に通し、化合物の分離および精製を行う手法です。本研究では、R.PabIの触媒反応によって遊離したアデニン塩基の検出に利用しました。
- 注6 マトリックス支援レーザー脱離イオン化飛行時間型質量分析
- 高分子化合物の分子量を決定する分析手法です。イオン化しやすいマトリックスをあらかじめサンプルと混合することにより、壊れやすい高分子化合物を安定的にイオン化し、その分子量を測定します。本研究では、R.PabIの触媒反応によって生じた産物DNAの分子量決定に利用しました。
- 注7 活性部位
- タンパク質は一本のポリペプチド鎖から作られる巨大分子で、それぞれ特徴的な立体構造を有しています。しかし、実際にその機能に関与する領域はごく一部で、その部位を活性部位といいます。タンパク質の機能には、この活性部位の構造が重要です。