牛の異常産を引き起こすウイルスの細胞内侵入機構の解明
- 発表者
-
村上 晋(東京大学大学院農学生命科学研究科 助教)
上間 亜希子(東京大学大学院農学生命科学研究科 特任助教)
小林 知也(東京大学大学院農学生命科学研究科 博士課程)
下島 昌幸(国立感染症研究所 ウイルス第一部第一室 室長)
加藤 健太郎(帯広畜産大学原虫病研究センター 准教授)
Massimo Palmarini(スコットランド グラスゴー大学MRCウイルス研究センター 教授)
堀本 泰介(東京大学大学院農学生命科学研究科 教授)
発表のポイント
◆牛に異常産を引き起こすアカバネ病ウイルスおよびシュマーレンベルグウイルスは細胞表面に発現しているヘパラン硫酸を介して細胞に結合、侵入していることがわかりました。
◆アカバネ病ウイルスおよびシュマーレンベルグウイルスはヘパラン硫酸の一種であるヘパリンによって感染が阻害されることがわかりました。
◆アカバネ病ウイルスおよびシュマーレンベルグウイルスと宿主との相互作用を担う分子メカニズムの理解に貢献する発見です。
発表概要
アカバネ病ウイルスおよびシュマーレンベルグウイルスは、共に妊娠している牛、羊、ヤギなどに感染すると胎仔の脳など中枢神経系で増殖し異常産を引き起こします。このアカバネ病ウイルスおよびシュマーレンベルグウイルスは牛から昆虫まで様々な細胞に感染することが可能ですが、細胞侵入のために必要な細胞の分子はこれまでわかっていませんでした。
今回、東京大学大学院農学生命科学研究科の村上晋助教、堀本泰介教授らは、ゲノム編集技術CRISPR /Cas9システムを用いてヘパラン硫酸ノックアウト細胞を作製し、ウイルスの感染におけるヘパラン硫酸の役割を調べました。その結果、ヘパラン硫酸が細胞におけるウイルス吸着・感染を促進するために重要な細胞接着因子であることを明らかにしました。
発表内容
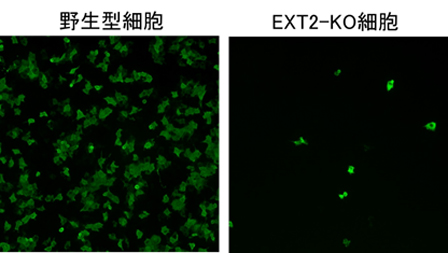
図1 ヘパラン硫酸を発現していない細胞(EXT2-KO)と野生型細胞へのアカバネウイルスの感染
緑色に染まっているのがウイルスに感染した細胞です。野生型細胞に比べてヘパラン硫酸が発現していない細胞では感染細胞数が非常に少ないのがわかります。
(拡大画像↗)
アカバネ病ウイルスおよびシュマーレンベルグウイルスは、共にブニヤウイルス科オルソブニヤウイルス属のウイルスです。これらのウイルスは遺伝学的に近縁であるだけでなくいくつかの共通した特徴を持っています、(1)妊娠している牛、羊、ヤギなどに感染すると関節症水頭症候群、流産等の異常産を引き起し、(2)胎仔の脳など中枢神経系(注1)で増殖し、(3)吸血昆虫であるヌカカ(注2)によって媒介されるためコントロールが難しい点です。一度これらのウイルス流行が始まると流行地域ではいわゆる流産の嵐(abortion storm)が起き、牛飼育農家などに大きな経済的な被害が出ます。アカバネ病ウイルスは日本を含む東アジア、東南アジア、オーストラリア、アフリカで流行しています。日本では毎年のように流行が確認されています。また、シュマーレンベルグウイルスは2011年にドイツのシュマーレンベルグで初めて発生が確認されて以来、たちまちヨーロッパの各国に広まり、甚大な経済被害がでました。このアカバネ病ウイルスおよびシュマーレンベルグウイルスは動物体内では神経細胞でよく増えますが、培養細胞レベルでは哺乳類である牛から昆虫まで様々な細胞に感染することが可能です。しかしながら、なぜそのような広い宿主域を持つのかということは明らかになっていません。
ヘパラン硫酸は多くの種類の細胞表面に発現し、細胞表面ではもっとも強いマイナス電荷を有する分子の一つです。これまでに多くのウイルスの細胞表面への接着にヘパラン硫酸が重要な役割を果たしていることがわかっています。本研究では、アカバネウイルスおよびシュマーレンベルグウイルス感染時におけるヘパラン硫酸の役割を明らかにすることを目的としました。
まず、培養細胞の表面のヘパラン硫酸を酵素処理で取り除き、アカバネウイルスあるいはシュマーレンベルグウイルスを感染させると、未処理の細胞と比較して感染率が大きく低下することがわかりました。また、ヘパラン硫酸の一種であるヘパリンがアカバネウイルスあるいはシュマーレンベルグウイルスの感染を阻害することがわかりました。これらの結果から、アカバネウイルスあるいはシュマーレンベルグウイルスの感染にはヘパラン硫酸が関与していることが示唆されました。
次に、より詳細に解析するために、ヘパラン硫酸を発現しない培養細胞を作製しました。今回はCRISPR/Cas9システムで培養細胞のヘパラン硫酸合成酵素であるEXT2遺伝子をノックアウトしました。このEXT2ノックアウト(EXT2-KO)細胞ではヘパラン硫酸が発現していないことを確認しました。次に、このEXT2-KO細胞にアカバネウイルスあるいはシュマーレンベルグウイルスを感染させると、野生型の細胞と比較して感染率が10倍以上低下することがわかりました(図1)。また、ウイルスの増殖もEXT2-KO細胞では野生型よりも低下していることがわかりました。さらに、EXT2-KO細胞に対するウイルスの吸着量をウイルスゲノムを指標としてRT-PCR法で定量したところ、EXT2-KO細胞では野生型のウイルスと比較して有意に減少していることがわかりました。EXT2-KO細胞にノックアウトしたEXT2遺伝子を再導入したところ、ウイルスの感染性が回復しました。これらの結果から、ヘパラン硫酸がアカバネウイルスおよびシュマーレンベルグウイルスの細胞侵入の際の重要な接着因子であることが明らかとなりました。
アカバネウイルスおよびシュマーレンベルグウイルスを始めとするオルソブニヤウイルスの生活環におけるウイルス-宿主間相互作用の機構は、未だほとんど明らかになっていません。今回、ウイルスの生活環を分子生物学的に明らかにしたことで、この機構を阻害する分子等がアカバネウイルスやシュマーレンベルグウイルス治療薬として応用できる可能性があります。
発表雑誌
- 雑誌名
- :「Journal of Virology」
- 論文タイトル
- :Heparan sulfate proteoglycan is an important attachment factor for cell entry of Akabane and Schmallenberg viruses
- 著者
- :Shin Murakami*, Akiko Takenaka-Uema, Tomoya Kobayashi, Kentaro Kato, Masayuki Shimojima, Massimo Palmarini, and Taisuke Horimoto*
- DOI番号
- :10.1128/JVI.00503-17
- 論文URL
- :http://jvi.asm.org/content/early/2017/05/18/JVI.00503-17.abstract
問い合わせ先
- 東京大学大学院農学生命科学研究科 獣医学専攻 獣医微生物学研究室
助教 村上 晋 - Tel:03-5841-5398
Fax:03-5841-8184 - Email:amurakam<アット>mail.ecc.u-tokyo.ac.jp <アット>を@に変えてください。
- 教授 堀本 泰介
Tel: 03-5841-5396
Email: ahorimo<アット>mail.ecc.u-tokyo.ac.jp <アット>を@に変えてください。 - 教授 堀本 泰介
用語解説
- 注1 中枢神経系
- 多数の神経細胞が集まっている領域で、哺乳類などの脊椎動物では脳と脊髄が中枢神経となる。
- 注2 ヌカカ
- ヌカカは、ハエ目ヌカカ科に属する昆虫で、体長が1から数mmほどの小型昆虫で、メスは蚊と同様に吸血する。アカバネウイルスやシュマーレンベルグウイルスは主にCulicoides属のヌカカによって媒介される。