細胞骨格と細胞膜の両方に結合してマクロピノサイトーシスを制御する情報伝達因子の発見
- 発表者
- 稲葉 弘哲 (東京大学大学院農学生命科学研究科応用生命工学専攻 博士課程学生:当時)
依田 幸司 (東京大学 名誉教授)
足立 博之 (東京大学大学院農学生命科学研究科応用生命工学専攻 准教授)
発表のポイント
◆細胞性粘菌(注1)のRap1(注2)の活性化因子であるGflBがマクロピノサイトーシスを制御することを明らかにしました。
◆GflBの細胞表層への局在化機構を明らかにし、この厳密な局在化がGflBの細胞内機能に必要であるというモデルを提唱しました。
◆マクロピノサイトーシスの制御機構の解明は癌などの病気の治療法の開発やドラッグデリバリーシステム(注3)への応用に繋がることが期待されます。
発表概要
マクロピノサイトーシス(マクロ飲作用)は細胞が比較的大きな容積の細胞外液を非特異的に取り込む現象で、細胞性粘菌などのアメーバからヒトまで進化的に良く保存されています。マクロピノサイトーシスはアクチン細胞骨格(注4)依存的で、アクチン細胞骨格が王冠状の突起(クラウン)を形成し、突起が閉じることで細胞外液を細胞内に取り込みます。しかし、マクロピノサイトーシスを制御する分子機構は未だによく分かっていません。
今回、東京大学農学生命科学研究科の稲葉弘哲博士課程学生(当時)と、同研究科の足立博之准教授らの研究グループは、マクロピノサイトーシスのモデル生物(注5)である細胞性粘菌を用い、マクロピノサイトーシスの制御因子としてRap1の活性化因子であるGflBを見出しました。
Rap1はヒトにも保存されている情報伝達因子であり、本研究は進化的に保存されたマクロピノサイトーシスの分子機構の解明に大きく寄与するものと考えられます。
発表内容
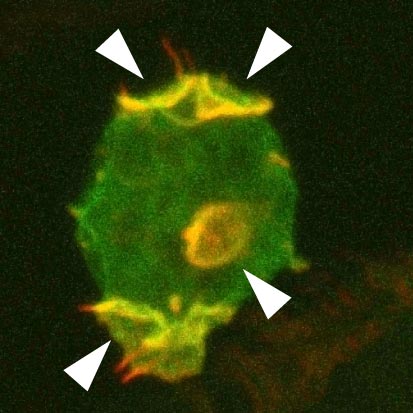
図1 GflB(緑)とアクチン線維(赤)の細胞内局在。GflBはアクチン線維と共に矢頭で示すマクロピノサイトーシスのための王冠状突起に強く局在し、その部分が黄色く見えている。
(拡大画像↗)
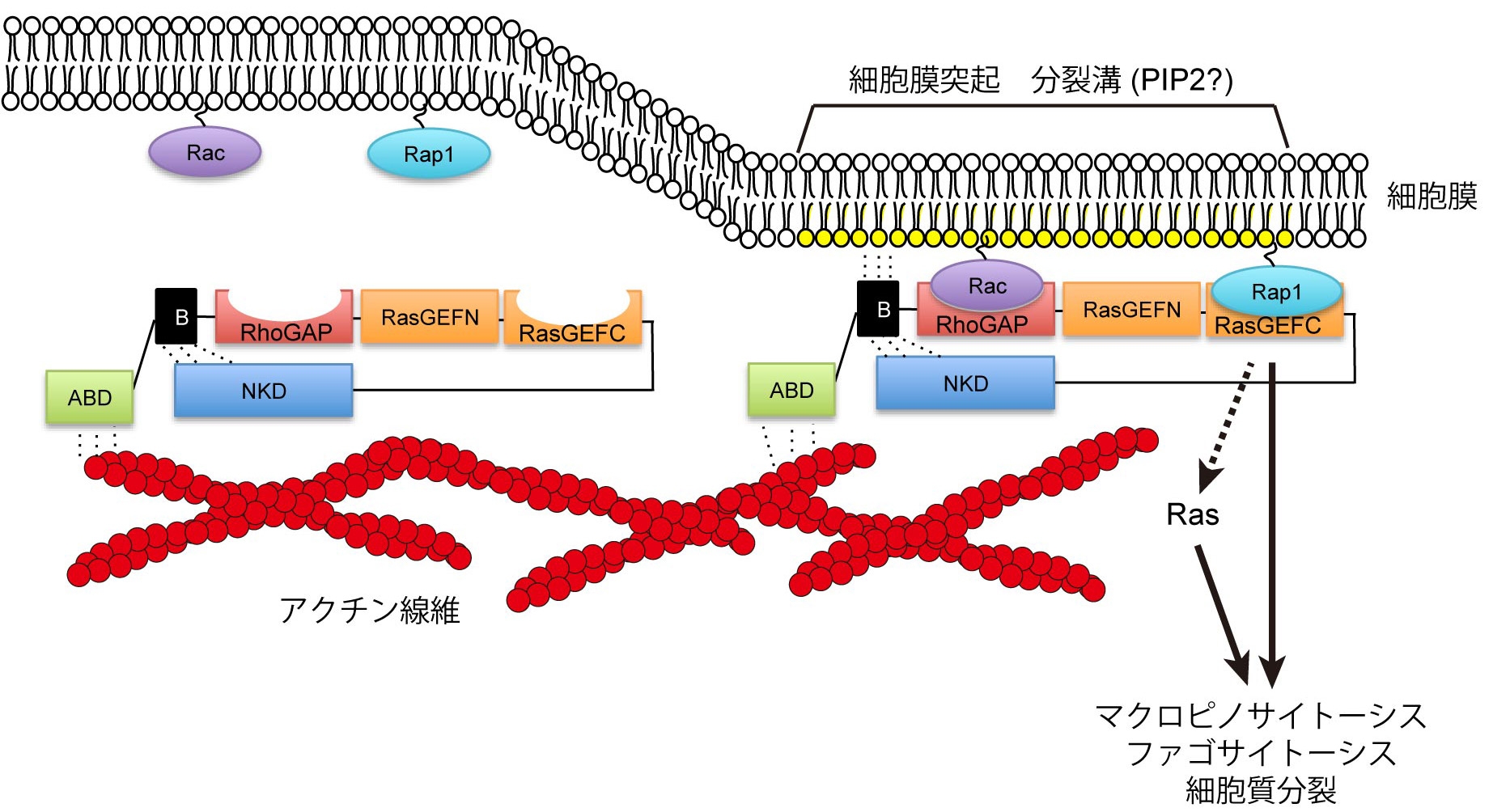
図2 GflBの局在化による活性化モデル。ABD:アクチン結合ドメイン、B:塩基性アミノ酸に富むドメイン、RhoGAP:低分子量Gタンパク質Racとの結合ドメイン、RasGEFN, RasGEFC:Rap1活性化ドメイン、NKD:nenkyrin domain(機能未知)。GflBはABDでアクチンと結合し、細胞表層に局在する。さらに、細胞膜脂質のPIP2やRacと結合することで、これらが存在する細胞膜の特定の部分でRap1やRasの活性を制御することで、マクロピノサイトーシス、ファゴサイトーシス、細胞質分裂に関与する。(拡大画像↗)
<研究の背景と目的>
細胞は、人間が飲食するのと同様に、細胞外の液体や固体を細胞内に能動的に取り込みます。これをエンドサイトーシスと呼び、取り込む物や機構によってピノサイトーシス(飲作用)とファゴサイトーシス(食作用)に大別されます。ピノサイトーシスの中でも比較的大きな容積の液体や、液中に含まれるやや大きめな固体を非特異的に取り込む現象をマクロピノサイトーシス(マクロ飲作用)と呼びます。この過程は、細胞に必要な栄養素や抗原の取り込みに機能していると考えられています。一方、ある種のがん細胞はマクロピノサイトーシスによる細胞外からの栄養分の取り込みを亢進(こうしん)することで、低栄養状態でも生存・増殖可能となっていることや、病原体が細胞内に進入する際にマクロピノサイトーシスを利用していることなどが最近明らかになり、病理学的にも重要であることが分かってきました。また、ドラッグデリバリーシステムにおいても、薬物の細胞への取り込みにマクロピノサイトーシスを利用することが考えられています。このようにマクロピノサイトーシスは現在注目を浴びており、その応用のためには詳細な分子機構を明らかにすることが重要です。
細胞性粘菌は自然界では微生物を餌として生活しており、ファゴサイトーシス能が発達しています。しかしながら、研究の都合上、バクテリアを含まない液体培地中での培養が可能となった変異株が多くの研究室で使われています。この変異株は、マクロピノサイトーシス能が発達しているため、マクロピノサイトーシスのモデル生物として用いられています。実際に、細胞性粘菌を使った研究からヒトまで保存されている多くの新しい知見が明らかになっています。
<研究の内容>
今回の研究で、足立博之准教授らのグループは細胞性粘菌Dictyostelium discoideumのGflBタンパク質に注目しました。GflBはアミノ酸配列の相同性から低分子量Gタンパク質の制御ドメインを持つことが予想されていました。まず、gflB遺伝子の破壊を行ったところ、gflBの遺伝子破壊株は親株と比べて細胞が細長く、大きな突起が数多く出ていることが分かりました。この突起の大部分はマクロピノサイトーシス時の王冠状突起であることが知られていたため、培地中に色素を加え、マクロピノサイトーシスの様子をタイムラプス観察しました。すると、gflB遺伝子破壊株ではこの突起の伸長、閉鎖、退縮の一連の過程、特に退縮の過程が親株と比べて非常に遅いことが分かりました。そこで、液体の取り込み速度を定量した結果、gflB破壊株では親株の1/3程度になっており、GflBが効率的なマクロピノサイトーシスに必要であることが明らかになりました。
また、GFPを用いた細胞内局在の観察においてもGflBが王冠状突起に局在することから(図1)、GflBのマクロピノサイトーシスへの関与が裏付けられました。さらに、遺伝子破壊株の解析や局在解析から、GflBはマクロピノサイトーシス以外にもファゴサイトーシスや細胞質分裂(注6)においても重要な機能を担っていることが明らかになりました。
次に、GflBの部分断片の局在を詳細に検討したところ、GflBのN末端領域はアクチン細胞骨格に局在し、N末端側の塩基性アミノ酸を多く含む領域は細胞膜を構成するリン脂質の一種であるPIP2(注7)が多く局在することが知られている膜領域に局在することが明らかになりました。このアクチン細胞骨格に局在するN末端領域は、ヒトまで保存されているアクチン結合ドメイン(villin headpiece domain: VHP)のアミノ酸配列と高い相同性を示し、試験管内でウサギ骨格筋由来のアクチン線維と直接結合することが明らかになりました。本研究及び他のグループから発表された結果を基に、図2に示す局所的な細胞膜におけるGflBの機能モデルを提唱しました。
<今後の予定・期待>
今回の結果や、他の研究グループの結果から、GflBはがん原遺伝子であるRas(注8)の活性も制御していることが示唆されました。Rasはマクロピノサイトーシスにおいて重要な機能を持つことが知られているため、GflBが直接Rasの活性を制御するのか、あるいはRap1を介して制御するのかを明らかにしていきたいと考えています。これまでRap1のマクロピノサイトーシスへの関与はヒトの細胞でも見出されていなかったため、ヒトの細胞でもRap1のマクロピノサイトーシスへの関与が明らかとなることが期待されます。
発表雑誌
- 雑誌名
- :「Journal of Cell Science」(2017年8月4日オンライン版)
- 論文タイトル
- :The F-actin-binding RapGEF GflB is required for efficient macropinocytosis in Dictyostelium
- 著者
- :Hironori Inaba, Koji Yoda, Hiroyuki Adachi*
- DOI番号
- :10.1242/jcs.194126
- 論文URL
- :http://jcs.biologists.org/content/early/2017/08/03/jcs.194126
問い合わせ先
- 東京大学大学院農学生命科学研究科
応用生命工学専攻 分子生命工学研究室
准教授 足立 博之 - Tel:03-5841-8139
Fax:03-5841-8139 - Email: adachih <at>mail.ecc.u-tokyo.ac.jp <at>を@に変えてください。
研究室URL:http://park.itc.u-tokyo.ac.jp/molbiotech/
用語解説
- 注1 細胞性粘菌
- 森の下生えなどに棲息し、バクテリアや酵母等の微生物を補食して増殖するアメーバ状の原生生物で、細胞運動の研究に用いられています。
- 注2 Rap1
- 細胞内で情報を下流に伝達する分子スイッチである低分子量Gタンパク質の一種で、細胞—細胞間結合や細胞—基質間結合を制御することで良く知られています。
- 注3 ドラッグデリバリーシステム
- 体内の薬物分布を量的・空間的・時間的に制御する薬物伝達システムのことで、副作用の軽減や、効果の増強といったメリットがあります。
- 注4 アクチン細胞骨格
- 細胞骨格は細胞の形態の維持や運動に必要な力を発揮するための繊維状の構造です。アクチン細胞骨格は主要な3つの細胞骨格の中の1つで、主に細胞膜直下に存在し、細胞形態の維持や、細胞膜突起の形成などに寄与します。
- 注5 モデル生物
- 普遍的な生命現象の研究に用いられる生物のことで、大腸菌、酵母、細胞性粘菌、線虫、ショウジョウバエ、アフリカツメガエル、シロイヌナズナ、マウスなどがあります。研究する現象に適した生物を選択し、研究者が同一のモデル生物を用いることで、より効率的に研究を進めることができます。
- 注6 細胞質分裂
- 細胞分裂の過程のうち、染色体を分配する核分裂に引き続いて起こる、細胞質を2つの娘細胞に分配する過程を指します。
- 注7 PIP2
- ホスファチジルイノシトール4,5-ビスリン酸のこと。細胞膜の微量な構成成分の1つで、様々な情報伝達経路において重要な役割を持っています。
- 注8 Ras
- 低分子量Gタンパク質の一種で、ras遺伝子の異常はがん化と関連することから、がん原遺伝子と呼ばれています。Rasは転写や細胞増殖、細胞運動などを制御することが知られています。