2つの反応を触媒するテルペン合成酵素の構造と反応機構を解明
- 発表者
-
富田武郎(東京大学生物生産工学研究センター 助教)
小林正弥(東京大学大学院農学生命科学研究科応用生命工学専攻 博士課程3年)
西山真(東京大学生物生産工学研究センター 教授)
葛山智久(東京大学生物生産工学研究センター 准教授)
発表のポイント
◆シクロラバンデュリルジリン酸の生合成酵素、CLDSの結晶構造とその反応機構を解明しました。
◆CLDSは、2つの分子間の縮合反応と分子内のプロトン転位が関与する環化反応によってシクロラバンデュリル骨格を構築することが明らかになりました。
◆CLDSによるテルペンの新しい生合成機構の解明により、新たなテルペン合成酵素の探索や酵素工学による有用テルペン化合物の創製が期待できます。
発表概要
シクロラバンデュリルジリン酸合成酵素(CLDS)は、放線菌Streptomyces sp. CL190から同定されたテルペン合成酵素であり、2分子のジメチルアリルジリン酸(DMAPP)の縮合反応とそれに続く環化反応を触媒することにより、シクロラバンデュリルジリン酸(CLPP)を生成します(図1)。CLDSのようなイソプレン基質の縮合と環化の両方の反応を同一酵素が触媒するテルペン合成酵素の報告例はなく、その反応機構も解明されていませんでした。
東京大学生物生産工学研究センターおよび大阪市立大学大学院理学研究科の共同研究グループは、重水素化基質を使用したラベル実験およびCLDSのX線結晶構造解析(注2)を実施し、シクロラバンデュリル骨格を構築するCLDSの詳細な触媒機構の解明に成功しました(図3)。
このような新しいテルペン生合成機構の発見は、自然界からの新たなテルペン合成酵素の探索、さらには酵素の機能改変によるテルペン化合物の構造多様性や生物活性の創出に寄与するものと考えられます。
発表内容
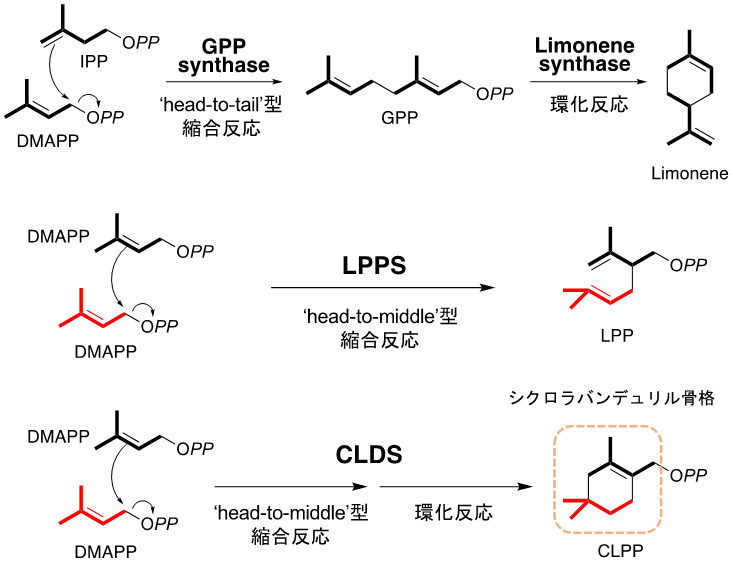
図1 テルペン合成酵素の例
head-to-tail型の縮合反応を触媒するGPP synthaseや、head-to-middle型のLPPSなどの鎖長伸長型テルペン合成酵素により、様々な長さのプレニルジリン酸が生成する。その後、テルペン環化酵素によって環状のテルペン骨格が形成される。CLDSはこれらの鎖長伸長と環化の両方の反応を触媒することで、シクロラバンデュリル骨格を有するCLPPを合成する。 (拡大画像↗)
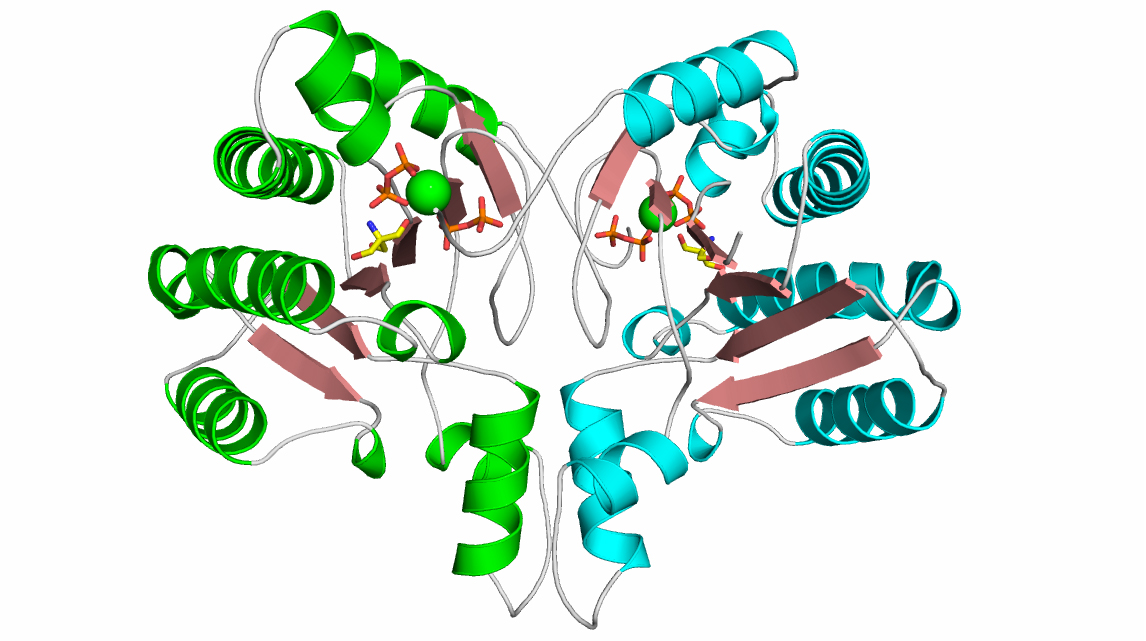
図2 CLDSの立体構造
cis-IDSに特有のホモ2量体構造からなり、活性中心にはMgイオン、Tris、2分子のピロリン酸が結合している。
(拡大画像↗)
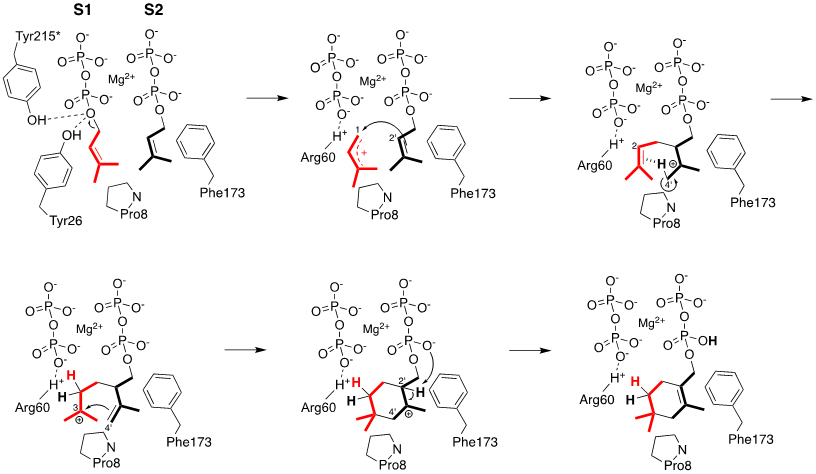
図3 CLDSの触媒する分子内プロトン転位とその推定反応機構
最初の縮合反応は、26番目のチロシンや215番目のチロシンと水素結合を形成しているS1サイトのDMAPP(赤色)のリン酸基の脱離により進行する。その後、4’位と2位間の分子内プロトン転位と求電子的閉環反応、およびリン酸基の酸素原子による2’位の脱プロトン化によりシクロラバンデュリル骨格が形成される。8番目のプロリンや173番目のフェニルアラニンはDMAPPの位置を制御することで、分子内プロトン転位を含む一連の反応を促進していると考えられる(拡大画像↗)
テルペン化合物(注1)は、イソプレン構造を基本単位とした天然物であり、縮合、環化、修飾などの反応を経ることで多様な構造と生物活性を生み出しています。とりわけテルペン骨格の構築を担う環化反応は、テルペン化合物の構造多様性を創出する上で極めて重要なファクターとなっています。CLDSは、放線菌Streptomyces sp. CL190の生産する抗腫瘍活性物質ラバンドシアニンの生合成研究の過程で見出されたテルペン合成酵素であり、2分子のDMAPPを基質として炭素数10の環状のシクロラバンデュリル骨格を有するCLPPを合成します(図1)。本酵素はcis型プレニルジリン酸合成酵素(cis-IDS)との相同性を示し、これらのファミリーに属する酵素としては、非環状のラバンデュリルジリン酸を合成するLPPS(図1)などが知られています。しかしながら、CLDSのように同一の酵素がイソプレン基質の縮合と環化の両方の反応を触媒するcis-IDSはCLDS以外に発見されていません。シクロラバンデュリル骨格を有する天然物は、放線菌以外に一部の植物においても見出されていますが、本骨格の生合成を担う酵素の報告例はCLDSのみにとどまっており、またその生合成機構も未解明でした。
CLDSの反応機構を詳細に調べるため、研究グループは重水素で標識した基質を用いたラベル実験、およびCLDSの立体構造に基づいて作製した変異酵素の機能解析を行いました。シクロラバンデュリル骨格の生合成は、2分子のDMAPPのhead-to-middle型の縮合、および反応中間体の環化による2段階の反応で進行すると予想しました。そこで、4位および5位メチル基のすべての水素原子を重水素原子に置換したラベル化DMAPPを用いて、CLDSの反応産物の標識パターンを解析しました。その結果、2分子のラベル化DMAPPに含まれる計12個の重水素がすべてCLPPに残り、かつ4’位の重水素が2位に転位していることが明らかになりました(図3)。
さらに研究グループは、X線結晶構造解析によってCLDSの立体構造の解明に成功しました(図2)。立体構造および構造に基づく変異体解析の結果から、CLDSはcis-IDSに共通の立体構造を有すること、また活性中心近傍の2つのアミノ酸残基(8番目のプロリン、173番目のフェニルアラニン)が環化反応に重要であることが判明しました(図3)。以上のラベル実験および立体構造の解析結果に基づき、CLDSの反応機構を図3のように推定しました。すなわち、まず2分子のDMAPPが縮合した後、4’位から2位へプロトンが分子内で転位します。その後、閉環反応と脱プロトン化によりCLPPが形成されると考えました。8番目のプロリンおよび173番目のフェニルアラニンのアミノ酸残基は、分子内プロトン転位を促進するように2分子のDMAPPの炭素鎖の配置を制御していると考えています。このような分子内プロトン転位が関与する反応例は、炭素数10個の環状テルペンを合成する環化機構としてはCLDSが最初の報告となります。
テルペン化合物は香料や医薬品などにおいて利用価値の高い化合物資源であり、その生合成機構を明らかにすることで、新しいテルペン骨格や有用な生物活性の創出に向けたさらなる知見を与えると考えられます。CLDSの触媒機構の解明により、自然界におけるテルペン環化反応の多様性の一端を示すことができたと同時に、新たなテルペン合成酵素の探索や改良、設計への貢献が期待されます。
本研究は、日本学術振興会の科学研究費補助金(15J10131, 26292058, 15K12758)、および科学研究費補助金新学術領域研究「生合成リデザイン」(16H06453, 17H05448)、A3 Foresight Programの支援を受けて行われました。
発表雑誌
- 雑誌名
- :Angewandte Chemie International Edition
- 論文タイトル
- :Structure and Mechanism of the Monoterpene Cyclolavandulyl Diphosphate Synthase that Catalyzes Consecutive Condensation and Cyclization
- 著者
- :Tomita Takeo ,1† Masaya Kobayashi,1† Yuma Karita,2 Yoko Yasuno,2 Tetsuro Shinada,2 Makoto Nishiyama,1 Tomohisa Kuzuyama1*
†Contributed equally.
1Biotechnology Research Center, The University of Tokyo
2Department of Material Science, Graduate School of Science, Osaka City University
- DOI番号
- :10.1002/anie.201708474
- 論文URL
- :http://onlinelibrary.wiley.com/doi/10.1002/anie.201708474/full
問い合わせ先
准教授 葛山 智久(くずやま ともひさ)
Tel: 03-5841-3073
Fax: 03-5841-8030
E-mail:utkuz<アット>mail.ecc.u-tokyo.ac.jp <アット>を@に変えてください。
研究室URL:http://park.itc.u-tokyo.ac.jp/biotec-res-ctr/saiboukinou/
用語解説
- 注1 テルペン化合物
- 炭素数5のイソプレンとよばれる化学構造を構成単位とする天然化合物の総称。ハッカに含まれるメントール、抗がん剤のタキソール、抗マラリア薬のアルテミシニンや抗酸化作用等を示すカロテノイド類が知られている。
- 注2 X線結晶構造解析
- タンパク質の結晶にX線を照射して得られる回折データをもとに、立体構造を原子レベルで解析する手法。